|
|
| (128 intermediate revisions not shown.) |
| Line 1: |
Line 1: |
| | <center>''' | | <center>''' |
| - | == '''H-RAS''' == | + | == '''HRAS''' == |
| | '''</center> | | '''</center> |
| - | <StructureSection load='4EFL' size='340' side='right' caption='Caption for this structure'> | + | |
| - | | + | |
| - | <center> '''
| + | <StructureSection load='4efl' size='340' side='left' caption='HRAS G domain complex with GPPNP and Mg+2 (PDB code [[4efl]])' scene='84/846756/Open/1'> |
| | + | |
| | + | |
| | + | <p dir='rtl'> |
| | + | החלבון HRAS מורכב מ 189 חומצות אמינו. בתהליך הגיבוש, לא גובש חלקו הסופי של החלבון בשל השונות הרבה המאפיינת אזור זה, לכן החלבון המגובש מורכב מ171 חומצות אמינו. |
| | + | בסצנה מימין מוצג החלבון כשהוא באינטראקציה עם ליגנד.<ref>PMID:22584058</ref> |
| | + | |
| | + | </p> |
| | + | |
| | + | <center> ''' |
| | + | == '''מבוא''' == |
| | + | ''' </center> |
| | + | <p dir='rtl'> |
| | + | החלבון HRAS בעל תפקיד חשוב במסלול הולכת אותות בתא. תהליך ביטוי גנים בתא מבוקר על מנת לבטא גנים הנחוצים לתא בזמן ספציפי ובפעילות מסוימת. תהליך הבקרה מתרחש באמצעות פקטורים שונים שהם לרוב חלבונים, המפעילים או מעכבים ביטוי גנים. הפעלת פקטורים אלו נעשית בשרשרת הולכת אותות אשר מתחילה בין היתר עם קשירה של ליגנד המגיע מחוץ לתא, לקולטן סמוך לחלבון HRAS. קשירת הליגנד לקולטן משפיעה על אקטיבציה של HRAS ומאפשרת לו לזרחן חלבונים שונים אשר במסלול הולכת אותות מפעילים גורמי שעתוק הנכנסים לגרעין ומשפיעים על ביטוי גנים. <br> החלבון HRAS משתייך למשפחת חלבוני G שהם בעלי תפקיד של [https://www.youtube.com/watch?v=eohda8jt7KM GTPase] |
| | + | , המבצעים הידרוליזה- פירוק של מולקולת GTP (Guanosine triphosphate) בעלת 3 קבוצות פוספט למולקולת GDP (Guanosine diphosphate) בעלת 2 מולקולות פוספט. החלבון RAS מופעל בעקבות סיגנל המגיע לתא, בעקבותיו הוא מפעיל מספר מסלולי הולכת אותות בתא אשר בסופו של דבר גורמים לשעתוק גנים הקשורים בוויסות תהליכי גדילת תאים. <br> |
| | + | התמונה הבאה ממחישה חלק ממסלול הולכת האותות המפעיל את החלבון HRAS |
| | + | <br> |
| | + | [[Image:RAS_מסלול_הולכת_אותות_המפעיל_את.png]] |
| | + | |
| | + | </p> |
| | + | |
| | + | |
| | + | <center> ''' |
| | + | == '''היסטוריה''' == |
| | + | ''' </center> |
| | + | <p dir='rtl'> |
| | + | החלבון HRAS משתייך למשפחת חלבוני RAS, שמה של משפחת חלבונים זו רומז לאופן גילוי החלבונים. בשנות השישים התגלו נגיפים מחוללי סרטן שגרמו לסרקומות- גידולים ברקמות חיבור בחולדות. חלבונים אלו נקראו Rat Sarcoma virus. שני האונקוגנים – גנים מחוללי סרטן, הראשונים שזוהו נקראו KRAS, ו HRAS, על שם החוקרים שגילו אותם Harvey& Kirsten. גן ras נוסף התגלה לאחר כ 20 שנה ונקרא NRAS כיון שהתגלה בתאים שנלקחו מגידול נוירובלסטומה. |
| | + | </p> |
| | + | |
| | + | <center> ''' |
| | == '''מבנה החלבון''' == | | == '''מבנה החלבון''' == |
| | ''' </center> | | ''' </center> |
| | | | |
| | <p dir='rtl'> | | <p dir='rtl'> |
| - | החלבון HRAS משמש תפקיד חשוב במסלול הולכת אותות בתא. הוא מעורב בוויסות תהליכי גדילה של תאים בתגובה לגירוי המגיע מגורמי גדילה. החלבון HRAS משתייך למשפחת חלבוני RAS בעלי תפקיד של GTPases , המבצעים הידרוליזה של מולקולת (Guanosine triphosphate) GTP- ל GDP-( Guanosine diphosphate) . | |
| | | | |
| - | <scene name='84/846756/Amino_acids/1'>החלבון מורכב מ- 189 חומצות אמינו</scene>, היוצרות <scene name='84/846756/Scondary_structure/1'>מבנה שניוני</scene> המכיל 6 משטחי β ו5 סלילי α. בחלבון ישנן <scene name='84/846756/Pospat/1'>עמדות שעוברות פוספורילציה</scene> <scene name='84/846756/Mag/1'>ועמדות לקשירת יון מגנזיום</scene>. עמדות הזרחון קשורות עם פעילות החלבון כחלק ממסלול הולכת האותות בתא. GTP. | + | <scene name='84/846756/Amino_acids/1'> החלבון שגובש מורכב מ-171 חומצות אמינו</scene>. המוצגות כאן כל אחת בצבע אחר. רצף חומצות האמינו יוצרות <scene name='84/846756/2/1'>מבנה שניוני </scene> המכיל 6 משטחי β ו 5 סלילי α. בסצנה משטחי β בחלבון מוצגים בצהוב וסלילי α מוצגים בורוד. בחלבון ישנם 12 אזורים שעוברים זרחון. |
| - | החלבון קשור בקצה C שלו לממברנת התא ,כך שליגנד המגיע מהסביבה החוץ תאית יכול להיקשר אל החלבון. חלקו האחר של החלבון נמצא בציטופלסמה ומשפיע על גורמים שונים האחראיים במסלול הולכת אותות ,על ביטוי גנים הקשורים בחלוקת התא.
| + | [https://he.wikipedia.org/wiki/%D7%96%D7%99%D7%A8%D7%97%D7%95%D7%9F זרחון] מתבצע על חומצות אמינו מסוג סרין, תריאונין וטירוזין היכולות לקבל קבוצת זרחה. |
| | + | <scene name='84/846756/Binding_mg/6'>חומצה אמינית סרין בעמדה 17 קושרת יון מגנזיום</scene>. יון המגנזיום מוצג בסצנה ככדור ירוק, נחוץ למבנה החלבון הקושר ליגנד, ולפעילותו כ- [https://www.hamichlol.org.il/%D7%97%D7%9C%D7%91%D7%95%D7%9F_G GTPase]. אתרים <scene name='84/846756/Gnp_binding/3'>17-23</scene> בחלבון אחראיים על קשירת הליגנד GNP. ליגנד זה משפיע על קשירה של החלבון HRAS עם חלבונים אחרים המשתתפים בתהליך האקטיבציה שלו. <ref>PMID:31988705</ref> |
| | + | האזור בחלבון <scene name='84/846756/Gtp_binding/4'>שקושר GTP,</scene> ומאופיין בפעילות של GTPase נמצא בציטופלסמה ומשפיע באמצעות זירחון על חלבונים שונים, האחראיים במסלול הולכת אותות, על ביטוי גנים הקשורים בחלוקת התא. |
| | + | <br> |
| | + | |
| | + | |
| | </p> | | </p> |
| | + | |
| | | | |
| | <center> ''' | | <center> ''' |
| Line 19: |
Line 53: |
| | ''' </center> | | ''' </center> |
| | | | |
| | + | <p dir='rtl'> |
| | | | |
| | + | |
| | + | HRAS מתפקד כמתג איתות בתוך התא, אשר משתתף במסלול הולכת אותות בתא המביא לגדילה וחלוקה של תאים. [https://www.youtube.com/watch?v=RqdlfZP26BI בסרטון הבא] ניתן לראות את החלבון HRAS במצב "כבוי" "ומופעל". במצב כבוי החלבון HRAS קשור ל- GDP ואילו במצב "מופעל" הוא קושר GTP. החלבון HRAS עובר אקטיבציה בעקבות סיגנל המגיע אל התא. בעקבות קשירת ליגנד לרצפטור מסוג טירוזין קינאז, טירוזין פנימי בקולטן עובר זרחון אשר בעקבותיו, מבנה הקולטן משתנה. כעת הקולטן מגייס חלבונים אשר עוברים גם הם שינוי קונפורמציה ויכולים לקשר בין הקולטן לחלבון HRAS. אחד משני חלבונים אלו מאקטב את HRAS, הוא משמש כ- GEF-(guanine nucleotide exchange factor), אשר מזרחן את HRAS דבר המוביל לשינוי קונפורמציית החלבון ובעקבות כך לשחרור מולקולת ה GDP מ HRAS. כתוצאה מכך, מתאפשרת קשירה מחדש של מולקולת GTP. כאשר החלבון HRAS קושר GTP הוא מגייס ומזרחן חלבון נוסף אשר מזרחן בתורו חלבונים אחרים, חלבונים אלו מפעילים פקטורי שעתוק המשפיעים על ביטוי גנים הקשורים לתהליכי גדילה והתמיינות של התא. |
| | + | <br> |
| | + | סוג אחר של חלבונים המשתתפים בתהליך הבקרה על HRAS אלו חלבוני GAP-(GTPase activating protein) המזרזים את הדה-אקטיבציה של HRAS, באמצעות זירוז שחרור קבוצת הזרחה הנוספת שבמולקולת GTP, כך ש HRAS נותר קשור ל GDP. |
| | + | <br> |
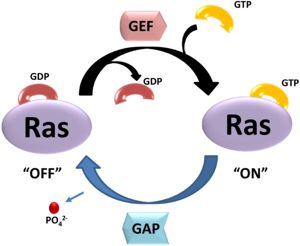
| | + | התמונה הבאה ממחישה את פעילות החלבונים GAP \ GEF בוויסות קשירת GDP או GTP בחלבון HRAS. |
| | + | [[Image:RAS.jpg|thumb|300px|left|<ref>PMID:31213978</ref> |
| | + | ]] |
| | + | |
| | + | |
| | + | |
| | + | </p> |
| | + | |
| | + | <center> ''' |
| | + | == '''מודפיקציות לאחר תרגום וחשיבותן''' == |
| | + | ''' </center> |
| | | | |
| | <p dir='rtl'> | | <p dir='rtl'> |
| | | | |
| - | HRAS מתפקד כמתג איתות בתוך התא , הוא מצוי במצב "מופעל" או "כבוי". במצב כבוי החלבון HRAS קשור ל GDPואילו במצב "מופעל" הוא קושר GTP. החלבון מכיל אזור אליו נקשר ליגנד, בעקבות קשירת הליגנד, החלבון עובר שינוי קונפורמציה המאפשר קשירת GTP. כאשר החלבון קושר GTPהוא מגייס חלבונים נוספים אשר משפיעים בשרשרת הולכת אותות בתא על ביטוי גנים הקשורים לתהליכי גדילה והתמיינות של התא.
| + | חלבונים עוברים שינויים לאחר תהליך התרגום, שינויים אלו מכונים מודפיקציות. מודיפיקציות על החלבון יכולת להיות תוספת של מולקולות אצטיל , מתיל, יוביקוויטין קבוצות זרחה ועוד. מודפיקציות אלו משפיעות על מבנה החלבון ומימלא גם על תפקודו בנוסף משמשות גם לתפקידי בקרה על פעילות החלבון. החלבון RAS עובר כמה מודפיקציות, בניהן תוספת קבוצות זרחה על חומצות אמינו סרין, תירוזין וטריאונין. בחלבון HRAS יש <scene name='84/846756/New_residue_of_posporilation/1'>12 עמדות</scene> שעוברות פסופורילציה. עמדות אלו בעלות חשיבות בבקרת פעילות החלבון HRAS. זרחון חומצה אמינית <scene name='84/846756/32/3'>טירוזין בעמדה 32</scene> <ref>PMID:25157176</ref> משפיע על מבנה החלבון באופן המאפשר קישור חלבונים שמגבירים את פעילות ה GTPase של החלבון HRAS ובכך מאיצים את קצב ההידרוליזה של GTP. דה-פוספורילציה <ref>PMID:31988705</ref>של טירוזין בעמדה זו |
| - | ישנם כמה חלבונים המשתתפים בתהליך האקטיבציה ודה-אקטיבציה של HRAS. חלבוני GAP-( GTPase activating protein) מזרזים את הדה-אקטיבציה של HRAS , באמצעות זירוז שיחרור קבוצת הזרחה הנוספת שבמולקולת GTP, כך שHRAS נותר קשור ל .GDP לעומת חלבוני GAP, חלבוני GEF-( guanine nucleotide exchange factor) מאקטבים את HRAS. תהליך קשירת GTP במקום GDP בחלבון HRAS מזורז על ידי חלבוני GEF אשר מזרזים את שחרור מולקולת הGDP מHRAS ומאפשרים קשירה מחדש של מולקולת GTP.
| + | מחזירה את החלבון למבנה הקודם שלו ומאפשרת קשירה של חלבונים המגבירים קשירת GTP בחלבון HRAS. |
| | + | <br> |
| | + | מודפיקציה נוספת בחלבון היא אצטילציה. לדוגמה, תוספת מולקולת אצטיל על חומצה אמינית <scene name='84/846756/104/2'>ליזין 104</scene> משפיעה על עיכוב הפעילות של HRAS. תוספת מולקולת האצטיל משנה את מבנה החלבון כך שנמנעת האינטראקציה עם GEF שגורם לחלבון לשחרר את מולקולת GDP ובמקומה לקשור GTP. <br> |
| | + | החלבון HRAS עובר מודפיקציה נוספת המבקרת את פעילותו, והיא מסוג יוביקוויטינציה. תוספת מולקולת יוביקוויטין (חלבון קטן בעל 76 חומצות אמינו) לחומצה אמינית מסוג ליזין במיקומים שונים בחלבון, משפיעה על מבנה החלבון באופן המשפיע על תפקודו. <scene name='84/846756/Ub/1'>בחלבון שגובש ניתן לראות 3 מתוך 4 אתרי יוביקוויטינציה בחלבון</scene> בהם מתווספת מולקולת יוביקוויטין. הוספת יוביקוויטין על חומצה אמינית <scene name='84/846756/Lys/3'>ליזין 117</scene> <ref>PMID:24247240</ref> משפעלת את החלבון HRAS. סימון במונויוביקוויטין על חומצה אמינית זו משפיע על מבנה החלבון HRAS באופן שמקדם שיחרור של מולקולת GDP דבר המאפשר קשירה מחודשת של GTP. |
| | + | |
| | | | |
| - | [[Image:RAS.jpg|thumb|400px]] | |
| | | | |
| | | | |
| | </p> | | </p> |
| | + | |
| | + | |
| | + | |
| | | | |
| | <center> ''' | | <center> ''' |
| - | == '''כאונקוגן RAS פעילות''' == | + | == '''כאונקוגן HRAS פעילות''' == |
| | ''' </center> | | ''' </center> |
| | | | |
| | <p dir='rtl'> | | <p dir='rtl'> |
| - | Ras הוא אחד [https://he.wikipedia.org/wiki/%D7%90%D7%95%D7%A0%D7%A7%D7%95%D7%92%D7%9F האונקוגנים]
| + | HRAS הוא אחד [https://he.wikipedia.org/wiki/%D7%90%D7%95%D7%A0%D7%A7%D7%95%D7%92%D7%9F האונקוגנים] |
| - | הבולטים ביותר במחלות סרטן אנושיות. מוטציות מסוימות בגן Ras גורמות לפעילות תמידית של חלבוני Ras ומביאות לביטוי יתר של מסלולי הולכת אותות בתא, המשפיעים על ביטוי גנים הקשורים בגדילה ובהתחלקות של התא. כתוצאה מכך מוטציות אלו עלולות לגרום למחלת הסרטן. | + | הבולטים ביותר במחלות סרטן אנושיות. מוטציות מסוימות בגן HRAS גורמות לפעילות תמידית של חלבוני HRAS ומביאות לביטוי יתר של מסלולי הולכת אותות בתא, המשפיעים על ביטוי גנים הקשורים בגדילה ובהתחלקות של התא. כתוצאה מכך מוטציות אלו עלולות לגרום למחלת הסרטן. |
| - | <br> שתי המוטציות האונקוגניות הנפוצות ביותר ב RAS הן מוטציות בחומצה אמינית גליצין, בעמדה 12 וחומצה אמינית גלוטמין, בעמדה 61. מוטציות אלו מעכבות במידה ניכרת את פעילות האנזים GTP ase דבר הגורם לחלבון להישאר במצב פעיל ("on") שהוא קשור ל GTP באופן קבוע. במצב פעיל RAS משתתף במסלול הולכת אותות בתא, אשר בסופם באים לידי ביטוי גנים הקשורים לחלוקת התא ולהישרדותו. <br> Ras הוא חלבון "טראנס ממברנאלי", חלקו נמצא מחוץ לממברנה ומשמש כרצפטור הקושר ליגנד. עם קשירת הליגנד, Ras עובר שינוי קונפורמציה- שינוי מבנה המשפיע על שינוי בתפקוד החלבון, וכעת החלבון מסוגל לקשור GTP ולהשתתף במסלול הולכת האותות בתא. ללא בקרה על פעילות החלבון RAS הוא משתתף במסלול הולכת אותות בתא באופן תמידי ומביא לביטוי קבוע של גנים הקשורים לחלוקת התא. כתוצאה מכך עלול להופיע ביטוי של גידול סרטני באורגניזם. | + | <br> שתי המוטציות האונקוגניות הנפוצות ביותר ב HRAS הן מוטציות בחומצה אמינית גליצין, בעמדה 12 וחומצה אמינית גלוטמין, בעמדה 61. <scene name='84/846756/Motetion/5'>מוטציות אלו</scene> מעכבות במידה ניכרת את פעילות האנזים GTP ase דבר הגורם לחלבון להישאר במצב פעיל ("on") -שהוא קשור ל GTP. |
| | + | <br> |
| | + | מוטציות אלו פוגעות באפשרות וויסות הפעילות של החלבון HRAS. במצב תקין, החלבון מופעל בעקבות סיגנל, כאשר ליגנד מחוץ לתא נקשר לקולטן על גבי ממברנת התא. בעקבות כך מגוייסים לקולטן חלבונים אשר משפיעים על קשירת GTP בחלבון HRAS ובכך מאקטבים אותו. כאשר HRAS פעיל, הוא מפעיל בשרשרת תהליכים חלבונים נוספים שמפעילים ביטוי גנים הקשורים בגדילת התא. כאשר החלבון עובר מוטציות כפי שתואר לעיל, החלבון כל הזמן קושר GTP ומפעיל באופן מתמשך, ביטוי גנים הקשורים בגדילת התא, גם ללא סיגנל המגיע מחוץ לתא. כתוצאה מכך עלול להופיע ביטוי של גידול סרטני באורגניזם. |
| | </p> | | </p> |
| | | | |
| Line 48: |
Line 107: |
| | <p dir='rtl'> | | <p dir='rtl'> |
| | | | |
| | + | תסמונת קוסטלו נגרמת כתוצאה מאחת מחמש מוטציות [https://genopedia.co.il/index.php/%D7%94%D7%95%D7%A8%D7%A9%D7%94_%D7%90%D7%95%D7%98%D7%95%D7%96%D7%95%D7%9E%D7%9C%D7%99%D7%AA_%D7%93%D7%95%D7%9E%D7%99%D7%A0%D7%A0%D7%98%D7%99%D7%AA דומיננטיות אוטוזומליות] שונות בגן HRAS הממוקם על כרומוזום 11. הווראציה הנפוצה ביותר, הקיימת בכ- 80% מהחולים, היא החלפה של חומצה אמינית גליצן בעמדה 12 בחומצה אמינית סרין. מוטציות בגן זה גורמות לייצור של חלבון HRAS לא תקין. החלבון המוטנטי אינו מעורר גדילת תאים בתגובה לאותות מסוימים מחוץ לתא, אלא פעיל |
| | + | באופן מתמשך ומשפיע על ביטוי גנים הקשורים לגדילה התמיינות וחלוקה של התאים בצורה בלתי מבוקרת, דבר העלול לעורר גידולים שפירים וגם סרטניים בגוף. |
| | + | [https://www.youtube.com/watch?v=mwXJbbJfmlM הסרטון הבא] מציג כיצד מתבטאת מוטציה בגן HRAS באדם. |
| | + | התסמונת משפיעה על מערכות מרובות בגוף, ובעלת תסמינים רבים. ביניהם, עיכובי גדילה לאחר הלידה, נמיכות קומה, עור רופף נוסף בצוואר, באצבעות, בכפות הידיים והרגליים, גידולים לא סרטניים (פפילומה) סביב הפנים ופי הטבעת, עיכוב התפתחותי, נכות שכלית, ומראה פנים אופייני. |
| | + | <br> |
| | | | |
| - | [https://www.youtube.com/watch?v=mwXJbbJfmlM תסמונת קוסטלו] | |
| | </p> | | </p> |
| - | | |
| - | </StructureSection> | |
| | | | |
| | | | |
| - | <scene name='84/846756/Pospat/1'>עמדות שעוברות פוספורילציה</scene> | + | <center> ''' |
| | + | == '''הפניות''' == |
| | + | ''' </center> |
| | | | |
| - | <scene name='84/846756/Mag/1'>ועמדות לקשירת יון מגנזיום</scene> | + | <references/> |
| | | | |
| - | == Disease == | + | <center> ''' |
| | + | == '''פעילות דידקטית''' == |
| | + | ''' </center> |
| | | | |
| - | == Relevance ==
| + | [http://proteopedia.org/wiki/index.php/Image:%D7%93%D7%A3_%D7%A2%D7%91%D7%95%D7%93%D7%94_%D7%9C%D7%AA%D7%9C%D7%9E%D7%99%D7%93_%D7%9C%D7%A2%D7%A8%D7%9A_HRAS.pdf דף עבודה לתלמיד] |
| - | | + | |
| - | == Structural highlights ==
| + | |
| - | | + | |
| - | | + | |
| - | | + | |
| - | == References ==
| + | |
| - | <references/>
| + | |
החלבון HRAS מורכב מ 189 חומצות אמינו. בתהליך הגיבוש, לא גובש חלקו הסופי של החלבון בשל השונות הרבה המאפיינת אזור זה, לכן החלבון המגובש מורכב מ171 חומצות אמינו.
בסצנה מימין מוצג החלבון כשהוא באינטראקציה עם ליגנד.[1]
מבוא
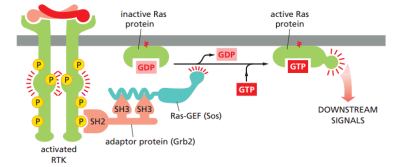
החלבון HRAS בעל תפקיד חשוב במסלול הולכת אותות בתא. תהליך ביטוי גנים בתא מבוקר על מנת לבטא גנים הנחוצים לתא בזמן ספציפי ובפעילות מסוימת. תהליך הבקרה מתרחש באמצעות פקטורים שונים שהם לרוב חלבונים, המפעילים או מעכבים ביטוי גנים. הפעלת פקטורים אלו נעשית בשרשרת הולכת אותות אשר מתחילה בין היתר עם קשירה של ליגנד המגיע מחוץ לתא, לקולטן סמוך לחלבון HRAS. קשירת הליגנד לקולטן משפיעה על אקטיבציה של HRAS ומאפשרת לו לזרחן חלבונים שונים אשר במסלול הולכת אותות מפעילים גורמי שעתוק הנכנסים לגרעין ומשפיעים על ביטוי גנים.
החלבון HRAS משתייך למשפחת חלבוני G שהם בעלי תפקיד של GTPase
, המבצעים הידרוליזה- פירוק של מולקולת GTP (Guanosine triphosphate) בעלת 3 קבוצות פוספט למולקולת GDP (Guanosine diphosphate) בעלת 2 מולקולות פוספט. החלבון RAS מופעל בעקבות סיגנל המגיע לתא, בעקבותיו הוא מפעיל מספר מסלולי הולכת אותות בתא אשר בסופו של דבר גורמים לשעתוק גנים הקשורים בוויסות תהליכי גדילת תאים.
התמונה הבאה ממחישה חלק ממסלול הולכת האותות המפעיל את החלבון HRAS
היסטוריה
החלבון HRAS משתייך למשפחת חלבוני RAS, שמה של משפחת חלבונים זו רומז לאופן גילוי החלבונים. בשנות השישים התגלו נגיפים מחוללי סרטן שגרמו לסרקומות- גידולים ברקמות חיבור בחולדות. חלבונים אלו נקראו Rat Sarcoma virus. שני האונקוגנים – גנים מחוללי סרטן, הראשונים שזוהו נקראו KRAS, ו HRAS, על שם החוקרים שגילו אותם Harvey& Kirsten. גן ras נוסף התגלה לאחר כ 20 שנה ונקרא NRAS כיון שהתגלה בתאים שנלקחו מגידול נוירובלסטומה.
מבנה החלבון
. המוצגות כאן כל אחת בצבע אחר. רצף חומצות האמינו יוצרות המכיל 6 משטחי β ו 5 סלילי α. בסצנה משטחי β בחלבון מוצגים בצהוב וסלילי α מוצגים בורוד. בחלבון ישנם 12 אזורים שעוברים זרחון.
זרחון מתבצע על חומצות אמינו מסוג סרין, תריאונין וטירוזין היכולות לקבל קבוצת זרחה.
. יון המגנזיום מוצג בסצנה ככדור ירוק, נחוץ למבנה החלבון הקושר ליגנד, ולפעילותו כ- GTPase. אתרים בחלבון אחראיים על קשירת הליגנד GNP. ליגנד זה משפיע על קשירה של החלבון HRAS עם חלבונים אחרים המשתתפים בתהליך האקטיבציה שלו. [2]
האזור בחלבון ומאופיין בפעילות של GTPase נמצא בציטופלסמה ומשפיע באמצעות זירחון על חלבונים שונים, האחראיים במסלול הולכת אותות, על ביטוי גנים הקשורים בחלוקת התא.
פעילות החלבון
HRAS מתפקד כמתג איתות בתוך התא, אשר משתתף במסלול הולכת אותות בתא המביא לגדילה וחלוקה של תאים. בסרטון הבא ניתן לראות את החלבון HRAS במצב "כבוי" "ומופעל". במצב כבוי החלבון HRAS קשור ל- GDP ואילו במצב "מופעל" הוא קושר GTP. החלבון HRAS עובר אקטיבציה בעקבות סיגנל המגיע אל התא. בעקבות קשירת ליגנד לרצפטור מסוג טירוזין קינאז, טירוזין פנימי בקולטן עובר זרחון אשר בעקבותיו, מבנה הקולטן משתנה. כעת הקולטן מגייס חלבונים אשר עוברים גם הם שינוי קונפורמציה ויכולים לקשר בין הקולטן לחלבון HRAS. אחד משני חלבונים אלו מאקטב את HRAS, הוא משמש כ- GEF-(guanine nucleotide exchange factor), אשר מזרחן את HRAS דבר המוביל לשינוי קונפורמציית החלבון ובעקבות כך לשחרור מולקולת ה GDP מ HRAS. כתוצאה מכך, מתאפשרת קשירה מחדש של מולקולת GTP. כאשר החלבון HRAS קושר GTP הוא מגייס ומזרחן חלבון נוסף אשר מזרחן בתורו חלבונים אחרים, חלבונים אלו מפעילים פקטורי שעתוק המשפיעים על ביטוי גנים הקשורים לתהליכי גדילה והתמיינות של התא.
סוג אחר של חלבונים המשתתפים בתהליך הבקרה על HRAS אלו חלבוני GAP-(GTPase activating protein) המזרזים את הדה-אקטיבציה של HRAS, באמצעות זירוז שחרור קבוצת הזרחה הנוספת שבמולקולת GTP, כך ש HRAS נותר קשור ל GDP.
התמונה הבאה ממחישה את פעילות החלבונים GAP \ GEF בוויסות קשירת GDP או GTP בחלבון HRAS.
מודפיקציות לאחר תרגום וחשיבותן
חלבונים עוברים שינויים לאחר תהליך התרגום, שינויים אלו מכונים מודפיקציות. מודיפיקציות על החלבון יכולת להיות תוספת של מולקולות אצטיל , מתיל, יוביקוויטין קבוצות זרחה ועוד. מודפיקציות אלו משפיעות על מבנה החלבון ומימלא גם על תפקודו בנוסף משמשות גם לתפקידי בקרה על פעילות החלבון. החלבון RAS עובר כמה מודפיקציות, בניהן תוספת קבוצות זרחה על חומצות אמינו סרין, תירוזין וטריאונין. בחלבון HRAS יש שעוברות פסופורילציה. עמדות אלו בעלות חשיבות בבקרת פעילות החלבון HRAS. זרחון חומצה אמינית [4] משפיע על מבנה החלבון באופן המאפשר קישור חלבונים שמגבירים את פעילות ה GTPase של החלבון HRAS ובכך מאיצים את קצב ההידרוליזה של GTP. דה-פוספורילציה [5]של טירוזין בעמדה זו
מחזירה את החלבון למבנה הקודם שלו ומאפשרת קשירה של חלבונים המגבירים קשירת GTP בחלבון HRAS.
מודפיקציה נוספת בחלבון היא אצטילציה. לדוגמה, תוספת מולקולת אצטיל על חומצה אמינית משפיעה על עיכוב הפעילות של HRAS. תוספת מולקולת האצטיל משנה את מבנה החלבון כך שנמנעת האינטראקציה עם GEF שגורם לחלבון לשחרר את מולקולת GDP ובמקומה לקשור GTP.
החלבון HRAS עובר מודפיקציה נוספת המבקרת את פעילותו, והיא מסוג יוביקוויטינציה. תוספת מולקולת יוביקוויטין (חלבון קטן בעל 76 חומצות אמינו) לחומצה אמינית מסוג ליזין במיקומים שונים בחלבון, משפיעה על מבנה החלבון באופן המשפיע על תפקודו. בהם מתווספת מולקולת יוביקוויטין. הוספת יוביקוויטין על חומצה אמינית [6] משפעלת את החלבון HRAS. סימון במונויוביקוויטין על חומצה אמינית זו משפיע על מבנה החלבון HRAS באופן שמקדם שיחרור של מולקולת GDP דבר המאפשר קשירה מחודשת של GTP.
כאונקוגן HRAS פעילות
HRAS הוא אחד האונקוגנים
הבולטים ביותר במחלות סרטן אנושיות. מוטציות מסוימות בגן HRAS גורמות לפעילות תמידית של חלבוני HRAS ומביאות לביטוי יתר של מסלולי הולכת אותות בתא, המשפיעים על ביטוי גנים הקשורים בגדילה ובהתחלקות של התא. כתוצאה מכך מוטציות אלו עלולות לגרום למחלת הסרטן.
שתי המוטציות האונקוגניות הנפוצות ביותר ב HRAS הן מוטציות בחומצה אמינית גליצין, בעמדה 12 וחומצה אמינית גלוטמין, בעמדה 61. מעכבות במידה ניכרת את פעילות האנזים GTP ase דבר הגורם לחלבון להישאר במצב פעיל ("on") -שהוא קשור ל GTP.
מוטציות אלו פוגעות באפשרות וויסות הפעילות של החלבון HRAS. במצב תקין, החלבון מופעל בעקבות סיגנל, כאשר ליגנד מחוץ לתא נקשר לקולטן על גבי ממברנת התא. בעקבות כך מגוייסים לקולטן חלבונים אשר משפיעים על קשירת GTP בחלבון HRAS ובכך מאקטבים אותו. כאשר HRAS פעיל, הוא מפעיל בשרשרת תהליכים חלבונים נוספים שמפעילים ביטוי גנים הקשורים בגדילת התא. כאשר החלבון עובר מוטציות כפי שתואר לעיל, החלבון כל הזמן קושר GTP ומפעיל באופן מתמשך, ביטוי גנים הקשורים בגדילת התא, גם ללא סיגנל המגיע מחוץ לתא. כתוצאה מכך עלול להופיע ביטוי של גידול סרטני באורגניזם.
תסמונת קוסטלו
תסמונת קוסטלו נגרמת כתוצאה מאחת מחמש מוטציות דומיננטיות אוטוזומליות שונות בגן HRAS הממוקם על כרומוזום 11. הווראציה הנפוצה ביותר, הקיימת בכ- 80% מהחולים, היא החלפה של חומצה אמינית גליצן בעמדה 12 בחומצה אמינית סרין. מוטציות בגן זה גורמות לייצור של חלבון HRAS לא תקין. החלבון המוטנטי אינו מעורר גדילת תאים בתגובה לאותות מסוימים מחוץ לתא, אלא פעיל
באופן מתמשך ומשפיע על ביטוי גנים הקשורים לגדילה התמיינות וחלוקה של התאים בצורה בלתי מבוקרת, דבר העלול לעורר גידולים שפירים וגם סרטניים בגוף.
הסרטון הבא מציג כיצד מתבטאת מוטציה בגן HRAS באדם.
התסמונת משפיעה על מערכות מרובות בגוף, ובעלת תסמינים רבים. ביניהם, עיכובי גדילה לאחר הלידה, נמיכות קומה, עור רופף נוסף בצוואר, באצבעות, בכפות הידיים והרגליים, גידולים לא סרטניים (פפילומה) סביב הפנים ופי הטבעת, עיכוב התפתחותי, נכות שכלית, ומראה פנים אופייני.
הפניות
- ↑ Muraoka S, Shima F, Araki M, Inoue T, Yoshimoto A, Ijiri Y, Seki N, Tamura A, Kumasaka T, Yamamoto M, Kataoka T. Crystal structures of the state 1 conformations of the GTP-bound H-Ras protein and its oncogenic G12V and Q61L mutants. FEBS Lett. 2012 Jun 12;586(12):1715-8. Epub 2012 May 11. PMID:22584058 doi:http://dx.doi.org/10.1016/j.febslet.2012.04.058
- ↑ Pantsar T. The current understanding of KRAS protein structure and dynamics. Comput Struct Biotechnol J. 2019 Dec 26;18:189-198. doi:, 10.1016/j.csbj.2019.12.004. eCollection 2020. PMID:31988705 doi:http://dx.doi.org/10.1016/j.csbj.2019.12.004
- ↑ Qu L, Pan C, He SM, Lang B, Gao GD, Wang XL, Wang Y. The Ras Superfamily of Small GTPases in Non-neoplastic Cerebral Diseases. Front Mol Neurosci. 2019 May 21;12:121. doi: 10.3389/fnmol.2019.00121., eCollection 2019. PMID:31213978 doi:http://dx.doi.org/10.3389/fnmol.2019.00121
- ↑ Bunda S, Heir P, Srikumar T, Cook JD, Burrell K, Kano Y, Lee JE, Zadeh G, Raught B, Ohh M. Src promotes GTPase activity of Ras via tyrosine 32 phosphorylation. Proc Natl Acad Sci U S A. 2014 Sep 9;111(36):E3785-94. doi:, 10.1073/pnas.1406559111. Epub 2014 Aug 25. PMID:25157176 doi:http://dx.doi.org/10.1073/pnas.1406559111
- ↑ Pantsar T. The current understanding of KRAS protein structure and dynamics. Comput Struct Biotechnol J. 2019 Dec 26;18:189-198. doi:, 10.1016/j.csbj.2019.12.004. eCollection 2020. PMID:31988705 doi:http://dx.doi.org/10.1016/j.csbj.2019.12.004
- ↑ Baker R, Wilkerson EM, Sumita K, Isom DG, Sasaki AT, Dohlman HG, Campbell SL. Differences in the regulation of K-Ras and H-Ras isoforms by monoubiquitination. J Biol Chem. 2013 Dec 27;288(52):36856-62. doi: 10.1074/jbc.C113.525691. Epub, 2013 Nov 18. PMID:24247240 doi:http://dx.doi.org/10.1074/jbc.C113.525691
פעילות דידקטית
דף עבודה לתלמיד
| |