This old version of Proteopedia is provided for student assignments while the new version is undergoing repairs. Content and edits done in this old version of Proteopedia after March 1, 2026 will eventually be lost when it is retired in about June of 2026.
Apply for new accounts at the new Proteopedia. Your logins will work in both the old and new versions.
DD-transpeptidase (Hebrew)
From Proteopedia
(Difference between revisions)
| Line 18: | Line 18: | ||
===<div style="text-align:right;direction:rtl;">'''תפקוד החלבון'''</div>=== | ===<div style="text-align:right;direction:rtl;">'''תפקוד החלבון'''</div>=== | ||
| - | [[Image:Peptide bond peptidoglycan.JPG|300 px|thumb|left|מבנה הפפטידוגליקן]] | + | [[Image:Peptide bond peptidoglycan.JPG|300 px|thumb|left|תמונה מס. 2: מבנה הפפטידוגליקן]] |
<p dir='rtl'> | <p dir='rtl'> | ||
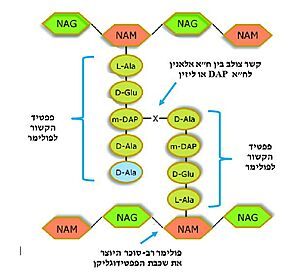
| - | האנזים טרנספפטידאז מעורב בבניית הדופן בתאי חיידקים, בזמן חלוקת התא. דופן התא היא מבנה קשיח המצוי מסביב לקרום תא החיידק, ובנוי ממולקולות פפטידוגליקן; פולימרים של רב-סוכר המחוברים בינהם בפפטידים קצרים. הפפטידים בין שכבות הפולימרים הרב-סוכריים נקשרים זה לזה בקשרים צולבים ומקנים לדופן מבנה תלת מימדי, יציב וקשיח. האנזים טרנספפטידאז אחראי על יצירת הקשרים הצולבים בין הפפטידים של שכבות הפפטידוגליקן<ref name="WIEZMANN">[https://bioteach.org.il/%D7%A2%D7%9C%D7%95%D7%A0%D7%99%D7%9D-2002/%D7%AA%D7%95%D7%9B%D7%9F-%D7%A2%D7%99%D7%95%D7%A0%D7%99/%D7%A0%D7%95%D7%A9%D7%90%D7%99-%D7%94%D7%A2%D7%9E%D7%A7%D7%94-1/%D7%97%D7%99%D7%99%D7%93%D7%A7%D7%99%D7%9D-%D7%95%D7%A0%D7%92%D7%99%D7%A4%D7%99%D7%9D-%D7%91%D7%92%D7%95%D7%A3-%D7%94%D7%90%D7%93%D7%9D/%D7%9E%D7%A7%D7%95%D7%A8%D7%95%D7%AA-%D7%9E%D7%99%D7%93%D7%A2-22/3573-%D7%A1%D7%A4%D7%A8-%D7%93%D7%99%D7%92%D7%99%D7%98%D7%9C%D7%99-%D7%97%D7%99%D7%99%D7%93%D7%A7%D7%99%D7%9D-%D7%95%D7%A0%D7%92%D7%99%D7%A4%D7%99%D7%9D-%D7%91%D7%92%D7%95%D7%A3-%D7%94%D7%90%D7%93%D7%9D-2016 כהנא, אורה. חיידקים ונגיפים בגוף האדם, 2016]</ref>. תגובה זו מתרחשת באתר הפעיל של האנזים, שבו חומצה אמינית סרין נקשרת לחומצה אמינית אלאנין הנמצאת בקצה הפפטיד בסובסטראט. האנזים מזרז את יצירת הקשר הפפטידי (סוג של [https://youtu.be/NgD9yHSJ29I?t=72 קשר קוולנטי] הנוצר בין חומצות אמינו) עם חומצת אמינו ליזין (בחיידקים גראם-חיוביים) או עם חומצת אמינו מסוג DAP (קיצור של: Diaminopimelic acid,זוהי חומצה אמינית לא שגרתית והיא נגזרת של החומצה האמינית ליזין בחיידקים גראם-חיוביים) הנמצאות בעמדה השלישית מהסוף בפפטיד המחובר לפולימר הסמוך. באופן זה נוצרים קשרים צולבים בין שכבות סמוכות בפפטידוגליקן, המקנים לדופן מבנה קשיח ויציב העמיד בפני לחץ אוסמוטי <ref name="PUBMED2">[https://pubmed.ncbi.nlm.nih.gov/14692773/ A mechanism-based inhibitor targeting the DD-transpeptidase activity of bacterial penicillin-binding proteins]</ref>. | + | האנזים טרנספפטידאז מעורב בבניית הדופן בתאי חיידקים, בזמן חלוקת התא. דופן התא היא מבנה קשיח המצוי מסביב לקרום תא החיידק, ובנוי ממולקולות פפטידוגליקן; פולימרים של רב-סוכר המחוברים בינהם בפפטידים קצרים. הפפטידים בין שכבות הפולימרים הרב-סוכריים נקשרים זה לזה בקשרים צולבים ומקנים לדופן מבנה תלת מימדי, יציב וקשיח. האנזים טרנספפטידאז אחראי על יצירת הקשרים הצולבים בין הפפטידים של שכבות הפפטידוגליקן<ref name="WIEZMANN">[https://bioteach.org.il/%D7%A2%D7%9C%D7%95%D7%A0%D7%99%D7%9D-2002/%D7%AA%D7%95%D7%9B%D7%9F-%D7%A2%D7%99%D7%95%D7%A0%D7%99/%D7%A0%D7%95%D7%A9%D7%90%D7%99-%D7%94%D7%A2%D7%9E%D7%A7%D7%94-1/%D7%97%D7%99%D7%99%D7%93%D7%A7%D7%99%D7%9D-%D7%95%D7%A0%D7%92%D7%99%D7%A4%D7%99%D7%9D-%D7%91%D7%92%D7%95%D7%A3-%D7%94%D7%90%D7%93%D7%9D/%D7%9E%D7%A7%D7%95%D7%A8%D7%95%D7%AA-%D7%9E%D7%99%D7%93%D7%A2-22/3573-%D7%A1%D7%A4%D7%A8-%D7%93%D7%99%D7%92%D7%99%D7%98%D7%9C%D7%99-%D7%97%D7%99%D7%99%D7%93%D7%A7%D7%99%D7%9D-%D7%95%D7%A0%D7%92%D7%99%D7%A4%D7%99%D7%9D-%D7%91%D7%92%D7%95%D7%A3-%D7%94%D7%90%D7%93%D7%9D-2016 כהנא, אורה. חיידקים ונגיפים בגוף האדם, 2016]</ref>. תגובה זו מתרחשת באתר הפעיל של האנזים, שבו חומצה אמינית סרין נקשרת לחומצה אמינית אלאנין הנמצאת בקצה הפפטיד בסובסטראט. האנזים מזרז את יצירת הקשר הפפטידי (סוג של [https://youtu.be/NgD9yHSJ29I?t=72 קשר קוולנטי] הנוצר בין חומצות אמינו) עם חומצת אמינו ליזין (בחיידקים גראם-חיוביים) או עם חומצת אמינו מסוג DAP (קיצור של: Diaminopimelic acid,זוהי חומצה אמינית לא שגרתית והיא נגזרת של החומצה האמינית ליזין בחיידקים גראם-חיוביים) הנמצאות בעמדה השלישית מהסוף בפפטיד המחובר לפולימר הסמוך (תמונה מס. 2). באופן זה נוצרים קשרים צולבים בין שכבות סמוכות בפפטידוגליקן, המקנים לדופן מבנה קשיח ויציב העמיד בפני לחץ אוסמוטי <ref name="PUBMED2">[https://pubmed.ncbi.nlm.nih.gov/14692773/ A mechanism-based inhibitor targeting the DD-transpeptidase activity of bacterial penicillin-binding proteins]</ref>. |
[[Image:Cross link peptidoglycan.jpg|500 px|יצירת הקשר הפפטידי]] | [[Image:Cross link peptidoglycan.jpg|500 px|יצירת הקשר הפפטידי]] | ||
</p> | </p> | ||
Revision as of 08:13, 25 January 2022
טרנספפטידאז
| |||||||||||
ביבליוגרפיה
- ↑ PDB
- ↑ UNIPROT
- ↑ The refined crystallographic structure of a DD-peptidase penicillin-target enzyme at 1.6 A resolution
- ↑ Wikipedia: DD-transpeptidase
- ↑ 5.0 5.1 כהנא, אורה. חיידקים ונגיפים בגוף האדם, 2016
- ↑ 6.0 6.1 A mechanism-based inhibitor targeting the DD-transpeptidase activity of bacterial penicillin-binding proteins
- ↑ ויקיפדיה: פניצילין
- ↑ ויקיפדיה: לקטאם