User:María Sánchez Morán/TFGParte3
From Proteopedia
| Line 23: | Line 23: | ||
<StructureSection load= size='350' side='right' caption='Estructuras propuestas por el grupo de Barber,' scene=''><scene name='90/902774/Abarber_msm/7'></scene> | <StructureSection load= size='350' side='right' caption='Estructuras propuestas por el grupo de Barber,' scene=''><scene name='90/902774/Abarber_msm/7'></scene> | ||
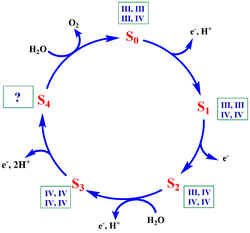
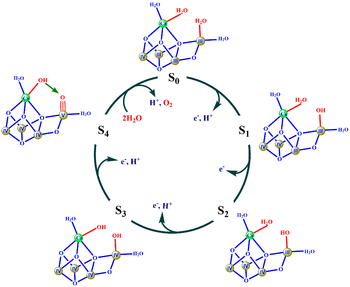
| - | + | [[Image:FigBMSM.png|thumb|350px|right| Fig. 4. Mecanismo propuesto por el grupo de Barber. En rojo, los cambios más significativos durante el ciclo catalítico. En círculos sombreados, los átomos de Mn con sus estados de oxidación expresados en números romanos. En verde, el átomo de Ca. Tomado de 18]] | |
| - | [[Image:FigBMSM.png|thumb|350px|right| Fig. Mecanismo propuesto por el grupo de Barber. En rojo, los cambios más significativos durante el ciclo catalítico. En círculos sombreados, los átomos de Mn con sus estados de oxidación expresados en números romanos. En verde, el átomo de Ca. Tomado de 18]] | + | |
Para desarrollar esta propuesta, el grupo de Barber se ha basado en las similitudes estructurales existentes entre el OEC y la enzima carbono monóxido deshidrogenasa que contiene hierro y níquel (Fe-Ni CODH). Esta enzima consiste en un cubano Fe<sub>3</sub>NiS<sub>4</sub> unido a un cuarto Fe vía puente de sulfuro, formando el clúster Fe<sub>4</sub>NiS<sub>5</sub>, que tiene un mecanismo conocido basado en un ataque nucleófilo catalizado por una base. [17] | Para desarrollar esta propuesta, el grupo de Barber se ha basado en las similitudes estructurales existentes entre el OEC y la enzima carbono monóxido deshidrogenasa que contiene hierro y níquel (Fe-Ni CODH). Esta enzima consiste en un cubano Fe<sub>3</sub>NiS<sub>4</sub> unido a un cuarto Fe vía puente de sulfuro, formando el clúster Fe<sub>4</sub>NiS<sub>5</sub>, que tiene un mecanismo conocido basado en un ataque nucleófilo catalizado por una base. [17] | ||
| - | En el caso del OEC, se propone la formación del enlace O-O como consecuencia de un ataque nucleófilo de un grupo hidroxilo, que se encuentra ligado al átomo de calcio, a un átomo de oxígeno con carácter electrófilo, unido a un manganeso en alto estado de oxidación. [17, 18] A continuación se presentan las características más importantes de este <scene name='90/902774/Abarber_msm/7'>mecanismo</scene>. | + | En el caso del OEC, se propone la formación del enlace O-O como consecuencia de un ataque nucleófilo de un grupo hidroxilo, que se encuentra ligado al átomo de calcio, a un átomo de oxígeno con carácter electrófilo, unido a un manganeso en alto estado de oxidación. [17, 18] A continuación se presentan las características más importantes de este <scene name='90/902774/Abarber_msm/7'>mecanismo</scene>, que también quedan reflejadas en la figura 4. |
*Este mecanismo depende de que Mn4 alcance un alto estado de oxidación en S<sub>4</sub> y, de esta forma, que el oxígeno unido a él sea deficiente electrónicamente. | *Este mecanismo depende de que Mn4 alcance un alto estado de oxidación en S<sub>4</sub> y, de esta forma, que el oxígeno unido a él sea deficiente electrónicamente. | ||
Revision as of 15:18, 8 February 2022
| |||||||||||