Phenol hydroxylase (hebrew)
From Proteopedia
| Line 29: | Line 29: | ||
<p dir='rtl'>החלבון הינו הומודימר, כלומר מורכב משתי תתי יחידות זהות, כל תת יחידה מכילה 665 חומצות אמינו. המבנה השניוני של החלבון מכיל מבני b sheet גדולים ומבני helix a. </p> | <p dir='rtl'>החלבון הינו הומודימר, כלומר מורכב משתי תתי יחידות זהות, כל תת יחידה מכילה 665 חומצות אמינו. המבנה השניוני של החלבון מכיל מבני b sheet גדולים ומבני helix a. </p> | ||
: <br> | : <br> | ||
| + | [[Image:pic2.png]] | ||
<p dir='rtl'>תת-היחידה של פנול הידרוקסילאז מורכבת משלושה דומיינים. שני הדומיינים הראשונים מהווים את האתר הפעיל וקושרים את הקו-פקטור ,FAD ואת הסובסטרט הפנולי, בעוד הדומיין הנוסף (השלישי) בעל תפקיד לא ידוע. </p> | <p dir='rtl'>תת-היחידה של פנול הידרוקסילאז מורכבת משלושה דומיינים. שני הדומיינים הראשונים מהווים את האתר הפעיל וקושרים את הקו-פקטור ,FAD ואת הסובסטרט הפנולי, בעוד הדומיין הנוסף (השלישי) בעל תפקיד לא ידוע. </p> | ||
: <br> | : <br> | ||
Revision as of 09:04, 20 February 2024
Contents |
Phenol hydroxylase
מידע כללי
מקור האנזים הינו מתאי שמר בשם cutaneotrichosporon cutaneum.
האנזים פנול הידרוקסילאז שייך למשפחת האנזימים פלווין (flavin enzymes), המכונים בדרך כלל הידרוקסילאזות ארומטיות. ידוע גם בשם, פנול 2-מונואוקסיגנאז. פעילותו של אנזים זה נחקרת, בין היתר, כיוון שנעשה בו שימוש נרחב בתעשיה בתהליכי טיהור סיבתיים ביולוגיים לפירוק וניטרול של פנולים. האנזים פועל על מגוון רחב של פנולים ותרכובות ארומטיות אחרות, ומופק בעיקר על ידי מיקרואורגניזמים, כולל חיידקים ופטריות. היכולת של מיקרואורגניזמים אלה לפרק פנולים הופכת אותם לכלים חשובים בתהליכי טיהור מים, כאשר מנסים להסיר מזהמים אורגניים מהסביבה. המקור הבלעדי של פנולים כמזהמים במים ובקרקע הוא זיהום תעשייתי או זיהום מדלקים. פנול הינו חומר שעלול לגרום לסרטן, בנוסף לכך גורם לבעיות אסתטיות, לטעם וריח חזקים.
פעילות אנזימתית
האנזים מזרז תגובת אוקסידציה של פנולים, הוספת קבוצת הידרוקסיל ל (OH-) למולקולת הפנול, ובכך ממיר אותה לקטכול (cathecol), תהליך שמהווה צעד ראשון חשוב במסלול הביודגרדציה של פנולים. האנזים מבצע תגובת חימצון/חיזור עם חמצן ומולקולת NADPH. בעזרת שתי מולקולות אלה נוצרת קבוצת הידרוקסיל המתחברת לטבעת הפנול וכך הופכת אותו לקטקול.
תרכובות הקטכול הנוצרות בעקבות האוקסידציה נוטות להיות פחות רעילות מהפנול המקורי ויותר מסיסות במים, דבר המקל על הסרתן מהסביבה. בפעילות האנזים מעורב הקו-פקטור FAD בתגובת החיזור (רדוקציה) של מולקולת חמצן.
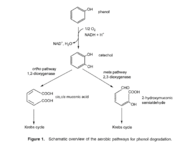
שמרים החיים בקרקע משתמשים באנזימים המכילים פלבין אדנין דינוקלאוטיד (FAD) להידרוקסילציה של פנולים. פנול הוא הסובסטרט הטוב ביותר, לפעילות הפנול הידרוקסילאז, אך האנזים מקבל גם פנולים פשוטים עם הידרוקסי-, אמינו-, הלוגן- או מתיל. תגובת ההידרוקסלציה מתחילה רצף מטבולי המאפשר את השימוש בתרכובת המתקבלות כמקור פחמן ואנרגיה. מולקולות הקטכול המתקבלות מומרות בתהליכים כימיים לתרכובות אורגניות שונות כגון אצטיל-CoA המשתלבות במעגל קרבס [1], H2O2.
גיבוש החלבון
האנזים פנול הידרוקסילאז גובש באופן מלא. בנוסף האנזים גובש יחד עם הקו-פקטור FAD ועם הסובסטרט פנול. מבנה הקריסטל שגובש מספק ראיות לשינוי מבני מתואם באנזים ובקואנזים שלו במהלך הקטליזה. החלבון גובש כארבע יחידות. .
מבנה החלבון
החלבון הינו הומודימר, כלומר מורכב משתי תתי יחידות זהות, כל תת יחידה מכילה 665 חומצות אמינו. המבנה השניוני של החלבון מכיל מבני b sheet גדולים ומבני helix a.
תת-היחידה של פנול הידרוקסילאז מורכבת משלושה דומיינים. שני הדומיינים הראשונים מהווים את האתר הפעיל וקושרים את הקו-פקטור ,FAD ואת הסובסטרט הפנולי, בעוד הדומיין הנוסף (השלישי) בעל תפקיד לא ידוע.
מיקום אתרים פעילים לקישור פנול: ח.אמינו 55, 290 אתרים פעילים קישור FAD: ח. אמינו 18-19, 43-45, 51-56, 118, 290,358, 368-376
מקורות מידע
שאלות
<>
| |||||||||||
- ↑ Hanson, R. M., Prilusky, J., Renjian, Z., Nakane, T. and Sussman, J. L. (2013), JSmol and the Next-Generation Web-Based Representation of 3D Molecular Structure as Applied to Proteopedia. Isr. J. Chem., 53:207-216. doi:http://dx.doi.org/10.1002/ijch.201300024
- ↑ Herraez A. Biomolecules in the computer: Jmol to the rescue. Biochem Mol Biol Educ. 2006 Jul;34(4):255-61. doi: 10.1002/bmb.2006.494034042644. PMID:21638687 doi:10.1002/bmb.2006.494034042644
Proteopedia Page Contributors and Editors (what is this?)
Nurit Ben Shimol, Rivka Cohen, Jonathan Guez, Michal Harel, Offir Lupo