1h6z (Italian)
From Proteopedia
Contents |
This is a placeholder
This is a placeholder text to help you get started in placing a Jmol applet on your page. At any time, click "Show Preview" at the bottom of this page to see how it goes.
Replace the PDB id (use lowercase!) after the STRUCTURE_ and after PDB= to load and display another structure.
| |||||||||
| 1h6z, resolution 3.00Å () | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Activity: | Pyruvate, phosphate dikinase, with EC number 2.7.9.1 | ||||||||
| |||||||||
| |||||||||
| Resources: | FirstGlance, OCA, PDBsum, RCSB | ||||||||
| Coordinates: | save as pdb, mmCIF, xml | ||||||||
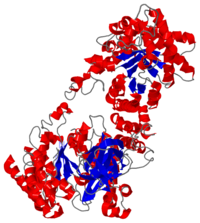
STRUTTURA CRISTALLOGRAFICA A 3.0 A DI RISOLUZIONE DELLA PYRUVATE PHOSPHATE DIKINASE GLICOSOMALE DI TRYPANOSOMA BRUCEI
La struttura cristallografica dell'enzima glicosomale pyruvate phosphate dikinase del parassita protozoario africano Trypanosoma brucei è stata risolta a 3.0 A di risoluzione per sostituzione molecolare. Il modello di ricerca era la struttura a 2.3 A di risoluzione dell'enzima di Clostridium symbiosum. A causa degli orientamenti relativi differenti degli domini e sub-domini nelle due strutture, la sostituzione molecolare non è potuta essere realizzata che posizionando questi elementi, quattro corpi in tutto, sequenzialmente nell'unità asimmetrica del cristallo di gruppo spaziale P2(1)2(1)2 che contiene una sub-unità della pyruvate phosphate dikinase (PPDK). Il modello affinato, comprendendo 898 residui e 188 molecole di solvente per sub-unità, ha un residuo cristallografico Rf =0.245 (fattore R libero Rfree =0.291), e mostra una stereochimica soddisfacente. Otto regioni, comprendendo un totale di 69 residui alla superficia della molecola, sono disordinate in questa forma cristallina. Le sub-unità di PPDK sono aggiustate intorno all'asse cristallografico di ordine 2 come un dimero, analogo a quell'osservato nell'enzima di C. symbiosum. Il paragone delle due strutture è stato effettuato da sovrapposizione dei due modelli. Sebbene il ripiegamento di ogni domain o sub-domain siano simili, gli orientamenti relativi di questi elementi costitutivi sono differenti nelle due strutture. L'enzima tripanosomale è "più ricurva" dell'enzima batterica, con la curvatura che aumenta dal centro della molecola, vicino all'asse di ordine 2 molecolare, verso la periferia dove il dominio N-terminale è localizzato. Conformemente a questa curvatura aumentata e delle differenti posizioni relative degli sub-domini, la fessura di legame del nucleotide nel dominio amino-terminale è più larga nella PPDK di T. brucei: il frammento N-terminale del dominio amino-terminale è localizzato a distanza del histidine catalitica 482, competente per la reazione di fosfo-trasferimento, pressappoco a 10 A di distanza. Le nostre osservazioni suggeriscono che le esigenze di movimenti di domini durante la catalisi per l'enzima potrebbero includere l'allargamento della fessura di legame del nucleotide, per permettere l'accesso e la partenza dei ligands AMP o ATP.
Riassunto tradotto da MEDLINE®/PubMed®, una banca dati del U.S. National Library of Medicine.
A proposito di questa struttura
1H6Z è una struttura a 1 catena di sequenza di Trypanosoma brucei. Dalle informazioni cristallografiche completi sono disponibili su OCA. Numeri biologici appropriati per questa proteina su B10NUMB3R5
Riferimenti
- Cosenza LW, Bringaud F, Baltz T, Vellieux FM. The 3.0 A resolution crystal structure of glycosomal pyruvate phosphate dikinase from Trypanosoma brucei. J Mol Biol. 2002 May 17;318(5):1417-32. PMID:12083528
- Cosenza LW, Bringaud F, Baltz T, Vellieux FM. Crystallization and preliminary crystallographic investigation of glycosomal pyruvate phosphate dikinase from Trypanosoma brucei. Acta Crystallogr D Biol Crystallogr. 2000 Dec;56(Pt 12):1688-90. PMID:11092947
- Bringaud F, Baltz D, Baltz T. Functional and molecular characterization of a glycosomal PPi-dependent enzyme in trypanosomatids: pyruvate, phosphate dikinase. Proc Natl Acad Sci U S A. 1998 Jul 7;95(14):7963-8. PMID:9653123
Page seeded by OCA on Mon May 25 07:47:17 2009