Resumen/Abstract
La fotólisis del agua es una reacción imprescindible para la vida en la Tierra. Consiste en una oxidación catalizada por el centro de formación de oxígeno (OEC), un complejo Mn4CaO5 localizado en el fotosistema II de los organismos fotosintéticos.
Se sabe que para la producción de O2 se necesitan cuatro impulsos luminosos. Estos impulsos provocan que el OEC pase por cinco estados principales (de S0 a S4) que se ha interpretado como un ciclo catalítico denominado ciclo de los estados S.
El objetivo de este trabajo es explorar las hipótesis existentes acerca de los mecanismos por los que la reacción podría llevarse a cabo y describir las estructuras por las que pasa el OEC. Para ello, se ha llevado a cabo una revisión bibliográfica y se han preparado modelos moleculares tridimensionales de dichas estructuras con objeto de comprender más fácilmente los cambios que implican los mecanismos posibles de una reacción de oxidación tan compleja.
Palabras clave: catálisis, centro de formación de oxígeno, fotosistema II, ciclo de estados S, estructura.
Water photolysis is an essential reaction for life on Earth. It is an oxidation catalysed by the oxygen-evolving complex (OEC), an Mn4CaO5 complex located in photosystem II of photosynthetic organisms.
It is known that four light flashes are required for O2 production. These flashes cause the OEC to pass through five main states (S0 to S4) and it has been interpreted as a catalytic cycle called the S-state cycle.
The aim of this project is to explore existing hypotheses for mechanisms by which the reaction could be carried out and to describe OEC structures along the process. For this purpose, a literature review has been carried out and three-dimensional molecular models of these structures have been prepared in order to facilitate the understanding of changes involved in such a complex oxidation reaction.
Keywords: catalysis, oxygen-evolving complex, photosystem II, S-state cycle, structure.
1. Introducción
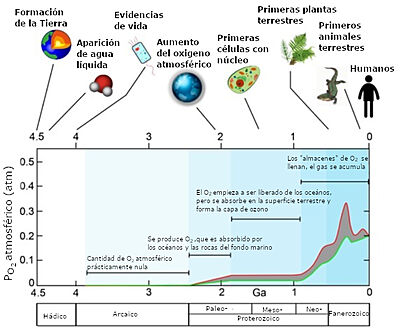
Fig. 1. Estimación superior (curva roja) e inferior (curva verde) de la cantidad de oxígeno acumulado en la atmosfera en una escala de miles de millones de años (Ga) y acontecimientos relevantes para el desarrollo de la vida en la Tierra. Adaptado de 3
1.1. Origen de los organismos fotosintéticos
La gran cantidad de O2 atmosférico distingue a la Tierra de los demás planetas del sistema solar y permite la existencia de los diferentes seres vivos en su superficie. Sin embargo, la atmósfera no siempre ha tenido esta composición. [1] Hace aproximadamente 3500 millones de años, la aparición de una metaloenzima capaz de fragmentar una molécula de H2O en O2, protones y electrones supuso un cambio drástico en la composición de la atmósfera. (Fig. 1) [2] Este hecho produjo una extinción masiva de las formas de vida existentes, para las que el oxígeno era un tóxico. Por otro lado, hubo un desarrollo de algunos organismos que utilizaban este oxígeno en su metabolismo, que fueron evolucionando hacia seres más complejos con células eucariotas y multicelulares. [3]
1.2. Metaloenzimas
Las metaloenzimas son macromoléculas formadas por un metal que actúa como ácido de Lewis y una proteína actuando como base de Lewis que tienen actividad enzimática. La funcionalidad de las diferentes biomoléculas es consecuencia de las estructuras y de la naturaleza metálica de cada caso. Así, los cambios conformacionales de las cadenas proteicas y las interacciones existentes en la biomolécula son los responsables de la acción del centro activo metálico.
En la formación de estas biomoléculas, lo más habitual es que los péptidos y proteínas se coordinen al átomo metálico por cesión electrónica de los grupos funcionales basados en átomos dadores de N, O ó S, generalmente de residuos o cadenas laterales de aminoácidos y en ocasiones de grupos prostéticos.
Los seres vivos dependen casi exclusivamente de las metalobiomoléculas para producir, a velocidades significativas, los procesos de transferencia electrónica necesarios en los organismos. Las consideraciones termodinámicas en este caso vienen dadas por los potenciales redox. Los diferentes ligandos y geometrías afectan al carácter redox del metal y al potencial redox del par. En cuanto a las consideraciones cinéticas, la biomolécula ofrece un entorno preformado al metal, determinado por el número y la orientación de los grupos dadores, que produce un estado entático: una situación energética muy favorable para que tenga lugar la reacción.
1.3. Centro de formación de oxígeno (OEC)
Cuando se comparan cianobacterias, algas y plantas contemporáneas, se observan un mismo centro inorgánico y un núcleo proteico similar en el centro activo de la enzima, lo que sugiere la creación natural de un único tipo de fotocatalizador hace unos 3500 millones de años llamado fotosistema II (PSII), [2] constituido por un complejo de múltiples subunidades proteicas que se localiza en el entorno lipídico de la membrana tilacoidal de algas, plantas y cianobacterias. [4]
El centro activo donde se produce la oxidación del H2O se conoce como complejo de formación de oxígeno (por sus iniciales en inglés, OEC, Oxygen Evolving Complex) y consiste en una pequeña agrupación de átomos o clúster formado por cuatro átomos de manganeso y un átomo de calcio unidos mediante átomos de oxígeno (Mn4CaO5). [5]
1.4. Importancia del proceso enzimático
La oxidación de la molécula de agua es una reacción difícil debido a la gran fortaleza de sus enlaces covalentes, reforzados por cierto carácter iónico resultado de la diferencia de electronegatividades existente entre los átomos de hidrógeno y el de oxígeno.
Desde el punto de vista termodinámico, el agua es muy estable y se necesita un oxidante muy fuerte para que se pueda llevar a cabo la reacción. Se trata de un proceso endotérmico y no espontáneo.
2H2O → O2 + 4H+ + e- E0=-1.23V ΔG0=482.4kJ/mol
Tampoco está favorecido desde el punto de vista cinético, debido a que la formación de O2 a partir de H2O es un proceso que necesita movilizar cuatro electrones. [5]
2. Materiales y métodos
Se ha realizado una búsqueda sistemática sobre el tema utilizando la base de datos SciFinder-n empleando las palabras clave “photosystem II”, “OEC”, “oxygen evolving complex” y “S-state cycle”, combinadas en algunos casos con “structure” y “function”. Los resultados de estas búsquedas fueron acotados en base al año de publicación y al número de citas.
Para las representaciones tridimensionales de las estructuras se han utilizado los siguientes programas:
Además, se ha preparado una versión en línea, complementaria a la memoria impresa, disponible en el portal Proteopedia, al que se puede acceder a través de: https://proteopedia.org/w/User:María_Sánchez_Morán/TFG
Índice |
Página Siguiente >>

