User:María Sánchez Morán/TFGParte2
From Proteopedia
| Line 29: | Line 29: | ||
<p style="font-size:16px;border-bottom:1px solid #ac9de3;background-color:#eae8f5;padding:3px;text-indent:5px;">3.3. Función</p> | <p style="font-size:16px;border-bottom:1px solid #ac9de3;background-color:#eae8f5;padding:3px;text-indent:5px;">3.3. Función</p> | ||
| - | El centro de reacción del fotosistema II se encarga fundamentalmente de eliminar electrones del H<sub>2</sub>O para formar O<sub>2</sub>. | + | El <scene name='90/902743/Oec2/1'>centro de reacción</scene> del fotosistema II se encarga fundamentalmente de eliminar electrones del H<sub>2</sub>O para formar O<sub>2</sub>. |
El PSII debe absorber un fotón con una longitud de onda de menos de 680nm para generar una pérdida de un electrón en la molécula de P<sub>680</sub>, produciendo P<sub>680</sub><sup>+</sup>. La P<sub>680</sub><sup>+</sup> es una clorofila oxidada del centro de reacción y tiene un gran poder oxidante. Su potencial de reducción es más positivo que el del agua, lo que permite llevar a cabo su oxidación para dar O<sub>2</sub> y H<sup>+</sup>. Esta oxidación es catalizada por el complejo de formación de oxígeno (OEC). [10] | El PSII debe absorber un fotón con una longitud de onda de menos de 680nm para generar una pérdida de un electrón en la molécula de P<sub>680</sub>, produciendo P<sub>680</sub><sup>+</sup>. La P<sub>680</sub><sup>+</sup> es una clorofila oxidada del centro de reacción y tiene un gran poder oxidante. Su potencial de reducción es más positivo que el del agua, lo que permite llevar a cabo su oxidación para dar O<sub>2</sub> y H<sup>+</sup>. Esta oxidación es catalizada por el complejo de formación de oxígeno (OEC). [10] | ||
Revision as of 14:41, 7 February 2022
| |||||||||||
4. Centro de formación de oxígeno
4.1.Estructura del centro metálico inorgánico: Mn4CaO5
El centro del clúster es un cubano (estructura donde los átomos se localizan en los vértices de un cubo) distorsionado formado por tres iones manganeso (denominados Mn1-Mn3), un ion Ca2+ y cuatro átomos de oxígeno (O1-O3 y O5). Hay, además, un cuarto ion manganeso (Mn4) localizado fuera del cubano y unido al resto de la estructura mediante dos μ-oxo puentes(enlaces en los que dos iones metálicos, en este caso iones manganeso, quedan unidos a través de un átomo de oxígeno) con los O4 y O5. [7]
Los cuatro iones metálicos pertenecientes al cubano se unen entre sí mediante μ-oxo puentes a tres átomos. Esta disposición encaja con las distancias metal-metal obtenidas experimentalmente: ~2.7Å para Mn-Mn y ~3.4 Å en el caso de Mn-Ca. La distancia entre el Mn4 y dos de los manganesos del cubano (Mn2 y Mn3) es de ~3.3Å, típica de los mono-μ-oxo puentes entre manganesos.[12] La del clúster completo es una silla distorsionada, donde el cubano representa la base y el Mn4 el respaldo.
La incorporación del Ca2+</sip> en el clúster provoca la distorsión de la estructura, puesto que las distancias Ca-O son mayores que las distancias Mn-O. Además, las distancias Mn-O5 son mucho mayores que el resto de las distancias Mn-O (similares a las distancias Mn-O de los óxidos de manganeso III y IV), lo que sugiere una unión débil entre el O5 y los iones manganeso cercanos.[7]
4.2.Ligandos
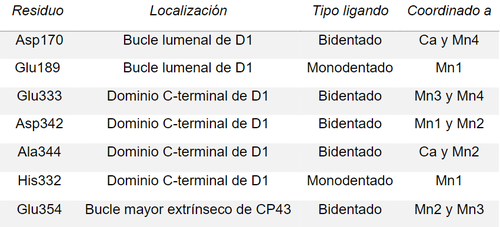
El clúster Mn4CaO5 está coordinado a seis residuos aminoácidos con grupos carboxilato y un residuo de histidina, los cuales se indican en la tabla 1.
Además de estos aminoácidos y de los puentes de oxígeno del cubano, el entorno de coordinación se satura con la presencia de cuatro moléculas de agua y un ion Cl-. Dos de estas moléculas de agua, W1 y W2, están coordinadas a Mn4; mientras que las dos restantes, W3 y W4, se coordinan al ion Ca2+. [4, 7, 14-16]
Tabla 1.
4.3. Segunda esfera de coordinación
Además de los ligandos que se coordinan directamente al clúster, se han encontrado tres residuos participantes en la segunda esfera de coordinación que podrían interaccionar con el centro metálico: D1-D61, D1-H337 y CP43-R357.
El ε-nitrógeno imidazol de D1-H337 se une mediante un enlace de hidrógeno directamente a O3, mientras que uno de los η-nitrógeno guanidina de CP43-R357 se une a O2 y O4, también mediante enlaces de hidrógeno. Además, el residuo η-nitrógeno guanidina de CP43-R357 está, a su vez, formando enlaces de hidrógeno con los residuos D1-C170 y D1-A344 de la primera esfera de coordinación.[5]
Por otro lado, uno de los oxígenos carboxilato de D1-D61 se enlaza directamente con W1, una de las moléculas de agua coordinadas a Mn4. El otro oxígeno carboxilato de D1-D61 interaccionacon W2 mediante enlaces de hidrógeno, esta vez indirectamente a través de otras dos moléculas de agua.
Todos estos enlaces de hidrógeno podrían estar implicados en la estabilización del clúster, aportando cargas parciales positivas que neutralicen las cargas negativas de los ligandos carboxilato y de los oxígenos. [14]