This old version of Proteopedia is provided for student assignments while the new version is undergoing repairs. Content and edits done in this old version of Proteopedia after March 1, 2026 will eventually be lost when it is retired in about June of 2026.
Apply for new accounts at the new Proteopedia. Your logins will work in both the old and new versions.
User:Carolina Castro Hernández/TFG/Parte5
From Proteopedia
12. Tropismo viral
En un principio se denomina tropismo tisular a la atracción altamente específica de un virus por un tejido específico del hospedador. En este caso, el tropismo se define como la afinidad del VIH por un correceptor específico en la superficie de las células que infecta (Villegas et al., 2004).
Durante la fase inicial de la infección, el VIH utiliza principalmente CCR5, mientras que el correceptor alternativo CXCR4 se utiliza más tarde en la infección cuando la enfermedad del SIDA va progresando en el individuo (Barmania y Pepper, 2013).
Este cambio fenotípico del tropismo viral se produce aproximadamente en un 50% de los individuos sintomáticos (Clapham y McKnight, 2001). Se debe a la modificación de unos pocos residuos en la gp120, tal como se ha demostrado en estudios in vitro. No obstante, estas modificaciones podrían ocurrir in vivo continuamente dada la alta tasa de error de la transcriptasa inversa (Chan et al., 1997).
Normalmente, el sitio de unión correceptor-gp120 no está completamente expuesto gracias a los bucles V1 y V2. Después de la unión de CD4 a la gp120 se produce la reorganización de dichos bucles y queda expuesto el sitio de unión al correceptor. Las mutaciones que confieren un fenotipo independiente de CD4 son precisamente aquellas que exponen desde un principio el sitio de unión al correceptor (Hoffman et al., 1999).
Diversos estudios han demostrado que el bucle V3 de la gp120 es determinante en el uso del correceptor y, por tanto, del tropismo viral (Hoffman y Doms, 1999). Los correceptores interactúan esencialmente con V3 que se compone de unos 35 aminoácidos (residuos 296-331) con un puente disulfuro entre residuos de cisteína en los extremos N y C-terminales (Masso y Vaisman, 2010) y posee una carga total positiva que varía de +2 a +10 (Cormier y Dragic, 2002).
Se han comparado distintas secuencias de V3 en VIH aislados que muestran la conservación de los segmentos N- y C-terminal así como la cresta con motivo GPG, en cuyos flancos se observa la variabilidad (Catasti et al., 1995). Esta cresta forma un giro beta y puede modular el uso del correceptor cuando se modifica su secuencia (Shimizu et al., 1999). La región flanqueante está formada por dos hebras antiparalelas de la β-lámina y es muy variable, de manera que puede alterar la superficie de acceso al correceptor y la estabilidad de la β-lámina (Catasti et al., 1995).
12.1 Modelo de conmutación del tropismo viral
Las regiones implicadas en la interacción con el correceptor se encuentran en los bucles variables V1/V2, V3 y parte de la lámina puente (Clapham y McKnight, 2001). La región entre las bases de los bucles V1/V2 y V3 de la gp120 conserva aminoácidos que podrían representar un dominio de unión capaz de interactuar con múltiples receptores de quimiocinas. Se ha propuesto un modelo en el que CD4 induce el movimiento de los bucles V1/V2 y V3, lo que facilita una interacción inicial con un receptor de quimiocinas específico y la exposición de este sitio de unión conservado, que se requiere para que ocurra la fusión (Rizzuto et al., 1998).
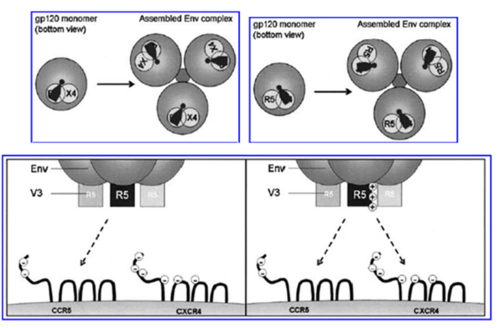
Las regiones cargadas positivamente en el lazo V3 tienen una fuerte interacción con los glicoproteínas de la superficie celular y por consiguiente, la promoción de la unión entre Env y CD4 y, a continuación, al correceptor específico. Por esta razón, se ha realizado un modelo simple de conmutación del tropismo viral (Fig. 4) mediante la alteración de la secuencia de V3. Algunas sustituciones en esa secuencia se realizan para modificar el sitio de unión para un correceptor, al mismo tiempo que se crea un nuevo sitio de unión para el otro correceptor (Hartley et al., 2005).
En los virus de tropismo X4, los residuos Asp97, Asp171, Asp187 (ECL-2), Asp193 y Asp262 del correceptor son esenciales para la unión de ligandos para CXCR4. Estos residuos están involucrados en la unión de CXCR4 y confieren carga negativa, aunque cada virus X4 aislado utiliza un conjunto de aminoácidos ligeramente distinto con el fin de ampliar la entrada en células diana (Dragic, 2001). En consecuencia, el uso de CXCR4 se asocia frecuentemente al aumento de cargas positivas en V3 (Cormier y Dragic, 2002).
La supresión del extremo N-terminal de CXCR4 tiene poco efecto en algunas cepas X4. Sin embargo, el ECL-2 es crítico para apoyar la entrada del virus y que además, según las investigaciones de Brelot et al. (1999), las cepas X4 varían la actividad de su correceptor con distintos residuos en el ECL-2 (Clapham y McKnight, 2001).
Por el contrario, el dominio N-terminal de CCR5 está cargado negativamente gracias a residuos de tirosina sulfatados y aminoácidos ácidos (Clapham y McKnight, 2001) que son sustituidos por Tyr89, Gly163, Ser179, Gln188 y Asn258, respectivamente (Tan et al., 2013), para formar el sitio de unión al correceptor CCR5 incluso asociándose también específicamente con residuos de la región C4/V3 de gp120.
No obstante, este modelo de conmutación del tropismo viral es bastante simple, dado que no tiene en cuenta los virus de tropismo dual (R5X4) que pueden utilizar ambos correceptores. Otra posibilidad es que se preserve la capacidad de participar al correceptor CCR5, al mismo tiempo que el aumento de la carga positiva neta por algunas sustituciones crea el sitio de unión de CXCR4 (Doranz et al., 1996).
12.2 Determinación del tropismo viral en individuos
La capacidad para modificar los residuos en secuencias implicadas en la unión de los correceptores es un mecanismo del VIH muy importante en evasión inmune (Clapham y McKnight, 2001). Las diferencias en la secuencia de aminoácidos y la conformación de C4/V3 pueden ser responsables de la especificidad del correceptor e igualmente, determinantes del tropismo viral (Dragic, 2001).
La acumulación de mutaciones en la región de interacción entre el correceptor y el bucle V3 de gp120 se relaciona con un cambio en la afinidad al correceptor debido a cambios en la secuencia de aminoácidos en posiciones 11 y 25 y/o a cambios conformacionales de V3 (Masso y Vaisman, 2010).
El primer algoritmo propuesto para la interpretación del tropismo fue la regla 11/25. Se basa en los aminoácidos básicos presentes en las posiciones 11 y 25, tales como arginina (R) o lisina (K), que se asocian con un uso del correceptor CXCR4 (tropismo X4). Su ausencia en dichas posiciones se relaciona con el uso de CCR5 (tropismo R5) (Isaka et al., 1999).
Utilizando esta regla se obtiene una sensibilidad del 30-40% y una especificidad del 80-90%, para la cepa X4 del virus. Se ha propuesto una modificación de esta regla para mejorar la sensibilidad que consiste en incluir la observación de la posición 24, resultando entonces en tropismo X4 cuando exista un aminoácido básico en posiciones 11, 24 y/ó 25, y en caso contrario, R5 (Cardozo et al., 2007).
Otra interpretación viene dada por la regla de la carga neta, basada en el cálculo de la carga total neta del lazo V3 de gp120 según la fórmula: (K + R) - (D + E). Si el resultado es inferior a cinco, se supone un tropismo R5, y si es igual o superior a cinco, X4. Al igual que la regla 11/25, esta regla muestra baja sensibilidad y alta especificidad para distinguir tropismos X4 (Poveda et al, s/f). Finalmente, si se combinan ambas reglas para distinguir el tropismo en el individuo mejora la sensibilidad al 88-93% y la especificidad al 96-100% para el uso del correceptor CXCR4 (IVAMI, 2009).
13. Terapias y perspectivas
Las investigaciones ponen de manifiesto el conocimiento de las estructuras moleculares de diversas proteínas de manera que se puede predecir la función de dichas proteínas y, por consiguiente, estudiar posibles dianas terapéuticas para combatir enfermedades causadas por distintos agentes. Al mismo tiempo, se pueden desarrollar nuevas técnicas de resolución de estructuras para continuar ampliando el conocimiento estructural y funcional.
El conocimiento de la estructura y función de Env y sus ligandos es vital debido a que Env es la única proteína de la superficie viral que media la entrada en las células.
Desde hace muchos años se considera un objetivo importante el sitio de unión de CD4 para bloquear la infección por VIH. Sin embargo, la comprensión del tropismo viral y las estructuras de los correceptores proporcionan nuevos conocimientos que tienen un gran impacto en el desarrollo de vacunas y fármacos anti-VIH.
A fecha de junio de 2015, 15,8 millones de personas tenían acceso al tratamiento antirretroviral (ONUSIDA, 2016). La terapia antirretroviral (TARV) puede dificultar la reproducción del virus cuando el individuo ya ha sido infectado. Los medicamentos antirretrovirales (ARV) más utilizados son inhibidores de las distintas enzimas que contiene el VIH. Conviene destacar los inhibidores nucleósidos (NRTI, en inglés) para inhibir la transcriptasa inversa y consecuentemente, para reducir la replicación del genoma vírico. Los fármacos dirigidos a bloquear la enzima integrasa del VIH previenen la inserción del genoma viral en el genoma celular, y los inhibidores de la proteasa permiten bloquear la fragmentación de los precursores de las proteínas virales (IAPAC, 1998; GTT-VIH, s/f).
Hasta la fecha, los individuos positivos para el VIH que han recibido el tratamiento antirretroviral de gran actividad (HAART, en inglés), que combina distintos medicamentos ARV, presentan una reducción muy eficaz de la carga viral. No obstante, existe la necesidad de desarrollar fármacos alternativos para las variantes resistentes o para individuos susceptibles a dichos fármacos.
Actualmente se están diseñando inhibidores de entrada tales como IT1t y Maraviroc (ya comentados en secciones anteriores) dirigidos a bloquear la interacción de la gp120 con el correceptor correspondiente. Además, un objetivo excelente para la investigación de vacunas es la mutación CCR5Δ32, puesto que los individuos homocigotos son resistentes a la infección.
Por otra parte, se debe tener en cuenta la mejora en las técnicas que permiten la resolución de estructuras y con ello, el conocimiento del fundamento a escala molecular de la función de las proteínas para favorecer el avance en las investigaciones de vacunas y fármacos que finalmente supongan una mejoría en la salud pública mundial.
14. Conclusión
Las glicoproteínas gp120 y gp41 de la envoltura del VIH son las principales encargadas de dirigir la infección viral y promover la enfermedad del SIDA. El conocimiento estructural de estas proteínas facilita también el conocimiento de su función, así como el desarrollo de líneas de actuación terapéutica.
Ambas glicoproteínas sufren cambios conformacionales drásticos, que median la entrada viral a la célula, inducidos por la unión de los distintos receptores y correceptores, los cuales también deben conocerse detalladamente para poder bloquear los mecanismos de infección por el VIH.
Se distingue un tropismo viral que es esencial para poder abordar distintas terapias adecuadas a cada individuo.
Las investigaciones deben proseguir en busca de mejoras para minimizar los efectos de la infección por VIH e incluso erradicar la enfermedad que produce.
15. Bibliografía
- Agrawal L, Lu X, Qingwen J, VanHorn-Ali Z, Nicolescu IV, McDermott DH, Murphy PM, Alkhatib G (2004). Role for CCR5Δ32 in resistance to R5, R5X4 and X4 human immunodeficiency virus type 1 in primary CD4+cells. Journal of Virology, 78:2277–87.
- Anderson JS, Javien J, Nolta JA, Bauer G (2009). Preintegration HIV-1 inhibition by a combination lentiviral vector containing a chimeric TRIM5 alpha protein, a CCR5 shRNA, and a TAR decoy. Molecular Therapy, 17:2103–14.
- Barmania F, and Pepper MS (2013). C-C chemokine receptor type five (CCR5): An emerging target for the control of HIV infection. Applied & Translational Genomics, 2:3–16. doi:10.1016/j.atg.2013.05.004.
- Brelot A, Heveker N, Adema K, Hosie MJ, Willett B, Alizon M (1999). Effect of mutations in the second extracellular loop of CXCR4 on its utilization by human and feline immunodeficiency viruses. Journal of Virology, 73:2576–86.
- Cardozo T, Kimura T, Philpott S, Weiser B, Burger H, and Zolla-Pazner S (2007). Structural basis for co-receptor selectivity by the HIV type 1 V3 loop. AIDS Research and Human Retroviruses, 23:415-426. doi:10.1089/aid.2006.0130.
- Catasti P, Fontenot JD, Bradbury EM, and Gupta G (1995). Local and global structural properties of the HIV-MN V3 loop. Journal of Biolgical Chemistry, 270:2224–32.
- Chan DC, Fass D, Berger JM, and Kim PS (1997). Core structure of gp41 from the HIV envelope glycoprotein Cell, 89: 263–273.
- Clapham PR, and McKnight A (2001). HIV-1 receptors and cell tropism. British Medical Bulletin, 58:43-59. doi: 10.1093/bmb/58.1.43.
- Combadiere C, Ahuja SK, Tiffany HL, Murphy PM (1996). Cloning and functional expression of CC CKR5, a human monocyte CC chemokine receptor selective for MIP-1a, MIP-1b and RANTES. Journal of Leukocyte Biology, 60:147–152.
- Cormier EG, and Dragic T (2002). The crown and stem of the V3 loop play distinct roles in human immunodeficiency virus type 1 envelope glycoprotein interactions with the CCR5 co-receptor. Journal of Virology, 76:8953–7. doi: 10.1128/JVI.76.17.8953-8957.2002.
- Cormier EG, Tran NDH, Yukhayeva L, Olson WC, and Dragic T (2001). Mapping the determinants of the CCR5 amino-terminal sulfopeptide interaction with soluble human immunodeficiency virus type 1 gp120-CD4 complexes. Journal of Virology, 75:5541-9.
- Császár A (2001). Involvement of polymorphisms in the chemokine system in the susceptibility for coronary artery disease (CAD). Coincidence of elevated Lp(a) and MCP-1–2518 G/G genotype in CAD patients. Atherosclerosis, 158:233–239. doi: 10.1016/S0021-9150(01)00423-3.
- Doranz BJ, Rucker J, Yi Y, Smyth RJ, Samson M, Peiper SC, Parmentier M, Collman RG, and Doms RW (1996). A dual-tropic primary HIV-1 isolate that uses fusin and the β-chemokine receptors CKR-5, CKR-3, and CKR-2b as fusion cofactors. Cell, 85:1149–58. doi: 10.1016/S0092-8674(00)81314-8.
- Dragic T (2001). An overview of the determinants of CCR5 and CXCR4 correceptor function. Journal of General Virology, 82:1807–1814. doi: 10.1099/0022-1317-82-8-1807.
- Edwards TG, Hoffman TL, Baribaud F, Wyss S, Labranche CC, Romano J, Adkinson J, Sharron M, Hoxie JA, and Doms RW (2001). Relationships between CD4 independence, neutralization sensitivity, and exposure of a CD4-induced epitope in a human immunodeficiency virus type 1 envelope protein. Journal of Virology, 75:5230-9. doi: 10.1128/JVI.75.11.5230–5239.2001.
- Faria NR, Rambaut A, Suchard MA, Baele G, Bedford T, Ward MJ, Tatem AJ, Sousa JD, Arinaminpathy N, Pépin J, Posada D, Peeters M, Pybus OG & Lemey P (2014). The early spread and epidemic ignition of HIV-1 in human populations. Science, 346:56-61. doi: 10.1126/science.1256739.
- Farzan M, Mirzabekov T, Kolchinsky P, Wyatt R, Cayabyab M, Gerard NP, Gerard C, Sodroski J, and Choe H (1999). Tyrosine sulfation of the amino terminus of CCR5 facilitates HIV-1 entry. Cell, 96:667-676. doi: 10.1016/S0092-8674(00)80577-2.
- González P, Álvarez R, Batalla A, Reguero JR, Álvarez V, Astudillo A, Cubero GI, Cortina A, and Coto E (2001). Genetic variation at the chemokine receptors CCR5/CCR2 in myocardial infarction. Genes and Immunity, 2:191–195.
- Grupping K, Selhorst P, Michiels J, Vereecken K, Heyndrickx L, Kessler P, Vanham G, Martin L, and Ariën KK (2012). MiniCD4 protein resistance mutations affect binding to the HIV-1 gp120 CD4 binding site and decrease entry efficiency. Retrovirology, 9:36. doi: 10.1186/1742-4690-9-3.
- GTT-VIH (s/f). Grupo de trabajo sobre tratamientos del VIH. Infovihtal 03. [Accedido: 08/06/16] Disponible en: http://gttvih.org/files/active/0/InfoV_esp_03_re.pdf
- Guttman M, Garcia NK, Cupo A, Matsui T, Julien JP, Sanders RW, Wilson IA, Moore JP, and Lee KK (2014). CD4-induced activation in a soluble HIV-1 Env trimer. Structure, 22:974–984.
- Hartley O, Klasse PJ, Sattentau QJ, Moore JP (2005). V3: HIV's switchhitter. AIDS Research and Human Retroviruses, 21:171-189. doi:10.1089/aid.2005.21.171.
- Hoffman TL, and Doms RW (1999). HIV-1 envelope determinants for cell tropism and chemokine receptor use. Molecular Membrane Biology, 16:57-65.
- Hoffman TL, LaBranche CC, Zhang W, Canziani G, Robinson J, Chaiken I, Hoxie JA, and Doms RW (1999). Stable exposure of the coreceptor-binding site in a CD4-independent HIV-1 envelope protein. Proceedings of the National Academy of Sciences USA, 96:6359–64.
- Hunt PW, Shulman NS, Hayes TL, Dahl V, Ma Somsouk, Funderburg NT, McLaughlin B, Landay AL, Adeyemi O, Gilman LE, Clagett B, Rodriguez B, Martin JN, Schacker TW, Shacklett BL, Palmer S, Lederman MM, and Deeks SG (2013). The immunologic effects of maraviroc intensification in treated HIV-infected individuals with incomplete CD41 T-cell recovery: a randomized trial. Blood, 121:4635-46.
- Hunt R (2010). Microbiología e Inmunología On-line. Capítulo 7. Universidad de Carolina del Sur, Facultad de Medicina. Columbia, SC, USA. Disponible en: http://www.microbiologybook.org/Spanish-Virology/spanish-chapter7-2.htm
- Hyde CL, MacInnes A, Sanders FA, Thompson JF, Mazzarella RA, Faergeman O, van Wijk D, Wood L, Lira M, and Paciga SA (2010). Genetic association of the CCR5 region with lipid levels in at-risk cardiovascular patients. Circulation: Cardiovascular Genetics, 3:162–168. doi: 10.1161/CIRCGENETICS.109.897793
- International Association of Providers of AIDS Care (IAPAC) (1998). [Accedido: 08/06/16]. Disponible en: http://www.aidsinfonet.org/fact_sheets/view/403?lang=spa
- Ioannidis JP, Rosenberg PS, Goedert JJ, Ashton LJ, Benfield TL, Buchbinder SP, Coutinho RA, Eugen-Olsen J, Gallart T, Katzenstein TL, Kostrikis LG, Kuipers H, Louie LG, Mallal SA, Margolick JB, Martinez OP, Meyer L, Michael NL, Operskalski E, Pantaleo G, Rizzardi GP, Schuitemaker H, Sheppard HW, Stewart GJ, Theodorou ID, Ullum H, Vicenzi E, Vlahov D, Wilkinson D, Workman C, Zagury JF, O'Brien TR (2001). Effects of CCR5-Δ32, CCR2-64I, and SDF-1 3′A alleles on HIV-1 disease progression: an international meta-analysis of individual-patient data. Annals of Internal Medicine, 135:782-95. doi: 10.7326/0003-4819-135-9-200111060-00008.
- Isaka Y, Sato A, Miki S, Kawauchi S, Sakaida H, Hori T, Uchiyama T, Adachi A, Hayami M, Fujiwara T, Yoshie O (1999). Small amino acid changes in the V3 loop of human immunodeficiency virus type 2 determines the coreceptor usage for CXCR4 and CCR5. Virology, 264:237-43.
- IVAMI (2009). VIH – Tropismo viral para receptores CCR5 y CXCR4. Secuenciación del gen de V3 para quasiespecies con tropismo CCR5 y CXCR4. [Accedido: 17/05/16]. Disponible en: http://www.ivami.com/resistencia-genotipica-de-vih-a-losantirretrovirales/793-vih-tropismo-viral-para-receptores-ccr5-y-cxcr4-secuenciacion-del-gen-de-v3-para-quasispecies-con-tropismo-ccr5-y-cxcr4
- Jie Cao, Louise Bergeron, Eirik Helseth, Markus Thali, Heinrich Repke, and Joseph Sodroski (1993). Effects of amino acid changes in the extracellular domain of the human immunodeficiency virus type 1 gp41 envelope glycoprotein. Journal of Virology, 67: 2747-55.
- Kwon YD, Finzib A, Wua X, Dogo-Isonagiec C, Leed LK, Mooree LR, Schmidta SD, Stuckeya J, Yanga Y, Zhou T, Zhu J, Vicice DA, Debnath AK, Shapiroa L, Bewleyc CA, Mascola JR, SodroskibJG , and Kwong PD (2012). Unliganded HIV-1 gp120 core structures assume the CD4-bound conformation with regulation by quaternary interactions and variable loops. Proceedings of the National Academy of Sciences USA, 109:5663-8. doi: 10.1073/pnas.1112391109.
- Kwong PD, Wyatt R, Robinson J, Sweet RW, Sodroski J, Hendrickson WA (1998). Structure of an HIV gp120 envelope glycoprotein in complex with the CD4 receptor and a neutralizing human antibody. Nature, 393:648-659.
- Kwong PD, Wyatt R, Sattentau QJ, Sodroski J, and Hendrickson WA (2000). Oligomeric modeling and electrostatic analysis of the gp120 envelope glycoprotein of human immunodeficiency virus. Journal of Virology, 74:1961–72.
- Labranche CC, Hoffman TL, Romano J, Haggarty BS, Edwards TG, Matthews TJ, Doms RW, and Hoxie JA (1999). Determinants of CD4 independence for a human immunodeficiency virus type 1 variant map outside regions required for co-receptor specificity. Journal of Virology, 73:10310-9.
- Liang M, Kamata M, Chen KN, Pariente N, An DS, Chen ISY (2010). Inhibition of HIV-1 infection by a unique short hairpin RNA to chemokine receptor 5 delivered into macrophages through hematopoietic progenitor cell transduction. The Journal of Gene Medicine, 12:255–265.
- Liu J, Bartesaghi A, Borgnia MJ, Sapiro G, and Subramaniam S (2008). Molecular architecture of native HIV-1 gp 120 trimers. Nature, 455:109–113. doi: 10.1038/nature07159.
- Martin L, Stricher F, Missé D, Sironi F, Pugnière M, Barthe P, Prado-Gotor R, Freulon I, Magne X, Roumestand C, Ménez A, Lusso P, Veas F, Vita C (2003). Rational design of a CD4 mimic that inhibits HIV-1 entry and exposes cryptic neutralization epitopes. Nature Biotechnology, 21:71-76.
- Masso M, and Vaisman II (2010). Accurate and efficient gp120 V3 loop structure based models for the determination of HIV-1 co-receptor usage. BMC Bioinformatics. doi: 10.1186/1471-2105-11-494.
- Merk A, and Subramaniam S (2013). HIV-1 envelope glycoprotein structure. Current Opinion in Structural Biology, 23:268–276.
- Munro JB, and Mothes W (2014). The HIV-1 Env trimer in HD. Structure, 22:935–936.
- Murphy PM, Baggiolini M, Charo IF, Herbert CA, Horuk R, Matsushima K, Miller LH, Oppenheim JJ, Power CA (2000). International Union of pharmacology. XXII. Nomenclature for chemokine receptors. Pharmacological Reviews, 52:145-176.
- Novina CD, Murray MF, Dykxhoorn DM, Beresford PJ, Riess J, Lee SK (2002). siRNA-directed inhibition of HIV-1 infection. Nature Medicine, 8:681–686.
- ONUSIDA (2016). Hoja informativa 2016. [Accedido: 06/05/16]. Disponible en: http://www.unaids.org/es/resources/fact-sheet
- Oppermann M (2004). Chemokine receptor CCR5: insights into structure, function and regulation. Cellular Signalling, 16:1201-1210.
- Organización Mundial de la Salud (2016). [Accedido: 06/05/16]. Disponible en: http://www.who.int/mediacentre/factsheets/fs360/es/
- Pancera M, Majeed S, Ban YE, Chen L, Huang CC, Kong L, Kwon YD, Stuckey J, Zhou T, Robinson JE, Schief WR, Sodroski J, Wyatt R, Kwong PD (2010). Structure of HIV-1 gp120 with gp41-interactive region reveals layered envelope architecture and basis of conformational mobility. Proceedings of the National Academy of Sciences, 107:1166-71. doi: 10.1073/pnas.0911004107.
- Pancera M, Zhou T, Druz A, Georgiev IS, Soto C, Gorman J, Huang J, Acharya P, Chuang GY, Ofek G, Stewart-Jones GBE, Stuckey J, Bailer RT, Joyce MG, Louder MK, Tumba N, Yang Y, Zhang B, Cohen MS, Haynes BF, Mascola JR, Morris L, Munro JB, Blanchard SC, Mothes W, Connors M, and Kwong PD (2014). Structure and immune recognition of trimeric prefusion HIV-1 Env. Nature, 514:455–461. doi: 10.1038/nature13808.
- Poveda E, Alcamí J, Paredes R, Córdoba J, Gutiérrez F, Llibre JM, Delgado R, Pulido F, Iribarren JA, Deltoro MG, Quero JH, Moreno S, y García F (s/f). Documento de consenso para la determinación genotípica del tropismo del VIH en la práctica clínica. [Accedido: 17/05/16]. Disponible en: http://www.vih-tropismo.com/consenso
- Ramírez DD (2015). Caracterización genotípica de la región C2-V3 de la molécula gp120 del VIH-1 y predicción del fenotipo viral. CD de Monografías, Universidad de Matanzas. [Accedido: 23/05/16]. Disponible en: http://monografias.umcc.cu/monos/2015/FCT/mo15262.pdf
- Rizzuto CD, Wyatt R, Hernández-Ramos N, Sun Y, Kwong PD, Hendrickson WA, Sodroski J (1998). A Conserved HIV gp120 glycoprotein structure involved in chemokine receptor binding. Science, 280:1949-53. doi: 10.1126/science.280.5371.1949.
- Ross TM, and Cullen BR (1998). The ability of HIV type 1 to use CCR3 as a co-receptor is controlled by envelope V1/V2 sequences acting in conjunction with a CCR-5 tropic V3 loop. Proceedings of the National Academy of Sciences USA, 95:7682–7686.
- Rottman JB, Ganley KP, Williams K, Wu L, Mackay CR, Ringler DJ (1997). Cellular localization of the chemokine receptor CCR5: correlation to cellular targets of HIV-1 infection. American Journal of Pathology, 151:1351.
- Samson M, Libert F, Doranz BJ, Rucker J, Liesnard C, Farber CM, Saragosti S, Lapoumeroulie C, Cognaux J, Forceille C, Muyldermans G, Verhofstede C, Burtonboy G, Georges M, Imai T, Rana S, Yi Y, Smyth RJ, Collman RG, Doms RW, Vassart G, Parmentier M (1996). Resistance to HIV-1 infection in caucasian individuals bearing mutant alleles of the CCR5 chemokine receptor gene. Nature, 382:722-5.
- Saphire EO, Parren PWHI, Pantophlet R, Zwick MB, Morris GM, Rudd PM, Dwek RA, Stanfield RL, Burton DR, Wilson IA (2001). Crystal structure of a neutralizing human IgG against HIV-1: A template for vaccine design. Science, 293:1155-9. doi: 10.1126/science.1061692.
- Shimizu N, Haraguchi Y, Takeuchi Y, Soda Y, Kanbe K, and Hoshino H (1999). Changes in and discrepancies between cell tropisms and correceptor uses of human immunodeficiency virus type 1 induced by single point mutations at the V3 tip of the env protein. Virology, 259:324–333.
- Szalai, C., Duba, J., Prohaszka, Z., Kalina, A., Szabo, T., Nagy, B., Horváth L, Tan Q, Zhu Y, Li J, Chen Z, Han GW, Kufareva I, Li T, Ma L, Fenalti G, Li J, Zhang W, Xie X, Yang H, Jiang H, Cherezov V, Liu H, Stevens RC, Zhao Q, & Wu B (2013). Structure of the CCR5 chemokine receptor–HIV entry inhibitor Maraviroc complex. Science, 341:1387-90. doi: 10.1126/science.1241475.
- Tan Q, Zhu Y, Li J, Chen Z, Han GW, Kufareva I, Li T, Ma L, Fenalti G, Li J, Zhang W, Xie X, Yang H, Jiang H, Cherezov V, Liu H, Stevens RC, Zhao Q, and Wu B (2013). Structure of the CCR5 Chemokine Receptor–HIV Entry Inhibitor Maraviroc Complex. Science, 341:1387-1390. doi: 10.1126/science.1241475.
- Villegas HHL, Turrent LCI, y Padilla CR (2004). El tropismo del VIH y su fenotipificación. Salus cum propositum vitae, Vol. 5, no. 4. Disponible en: http://www.respyn.uanl.mx/v/4/ensayos/tropismo_vih.htm
- Westby M, Lewis M, Whitcomb J, Youle M, Pozniak AL, James, IT, Jenkins TM, Perros M, and Ryst EVD (2006). Emergence of CXCR4-using human immunodeficiency virus type 1 (HIV-1) variants in a minority of HIV-1-infected patients following treatment with the CCR5 antagonist maraviroc is from a pretreatment CXCR4-using virus reservoir. Journal of Virology, 80:4909–4920. doi: 10.1128/JVI.80.10.4909-4920.2006
- Wu B, Chien EYT, Mol CD, Fenalti G, Liu W, Katritch V, Abagyan R, Brooun A, Wells P, Bi FC, Hamel DJ, Kuhn P, Handel TM, Cherezov V, and Stevens RC (2010). Structures of the CXCR4 chemokine GPCR with small-molecule and cyclic peptide antagonist. Science, 330:1066-71. doi: 10.1126/science.1194396.